一、元素
1.概念
元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
说明:
(1)决定元素种类的是质子数(核电荷数),与中子数、核外电子数无关。
(2)必须要强调是“一类原子”,而不能说成 “粒子” 。
(3)元素是一个宏观概念,只论“种”,不论“个”。
(4)已发现的元素只有100余种,但组成的物质已超过3000万种。
2.元素与原子的区别和联系
| 元 素 | 原 子 | |
| 概念 | 具有相同核电荷数的一类原子的总称。 | 化学变化中的最小粒子。 |
| 区别 | 只讲种类,不讲个数,没有数量多少的含义。 | 既讲种类,又讲个数,有数量多少的含义。 |
| 使用范围 | 用于描述物质的宏观组成。 | 用于描述物质的微观构成。 |
| 举例 | 如:水中含有氢元素和氧元素。即,水是由氢元素和氧元素组成的。 | 如:一个水分子,是由两个氢原子和一个氧原子构成的。 |
| 联系 |  | |
3.元素的分类
(1)金属元素,中文名称通常具有“钅”偏旁,只有汞除外。
(2)非金属元素,中文名称通常具有“石”、“氵”或“气”偏旁,如碳、溴、氧等。
(3)稀有气体元素,包括氦、氖、氩等。
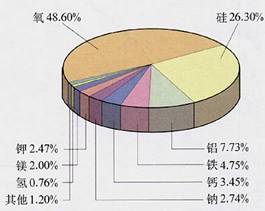
4.地壳中元素的质量分数
地壳是指地球外表一层由岩石组成的固体硬壳,其中元素的含量排序前五位是:氧、硅、铝、铁、钙。
二、元素符号
1.元素符号的意义:
(1)表示一种元素。 (2)表示这种元素的一个原子。
2.写法、读法
(1)读法:化学元素的读音,一般都是按照偏旁字来发音的。例如,镁读作“美”,锂读作“里”,碘读作“典”等等。但也有不少例外,如氧读作“养”,钠读作“纳”,溴读作“嗅”等等。
(2)写法:根据化学元素的拉丁文名称的首字母或者前几个字母来确定。在书写时,注意一大二小,即第一个字母大写,第二个字母小写。
三、元素周期表
根据元素的原子结构和性质,把现在已知的一百多种元素按原子序数(核电荷数)依次递增的顺序排列起来,这样得到的表叫元素周期表。在周期表中,还用不同的颜色对金属元素、非金属元素做了分区。
1.元素周期表的结构:
每一格:在元素周期表中,每一种元素均占据一格。对于每一格,均包括原子序数、元素符号、元素名称、相对原子质量等内容。
每一横行(周期):元素周期表的每一横行叫做一个周期,共有7个横行,有7个周期。
说明:每周期开头是金属元素(第一周期除外),靠近尾部的是非金属元素,结尾的是稀有气体元素。这说明随着原子序数的递增,元素原子的最外层上的电子数由1个递增到8个,达到稀有气体元素原子的稳定结构,然后又重复出现原子最外层电子数从1个递增到8个的变化规律。这种规律性的变化也就是“元素周期表”的名称的来源,它反映了元素之间的内在联系。
每一纵行(即族):元素周期表的18个纵行中,除第8、9、10三个纵行共同组成一个族外,其余15个纵行,每一个纵行叫做一族,共有16个族。
2.元素周期表的意义:
学习和研究化学的重要工具;为寻找新元素提供了理论依据;由于在元素周期表中位置越靠近的元素性质越相似,可以启发人们在元素周期表的一定的区域寻找新物质(如农药、催化剂、半导体材料等)。
【资料介绍】元素周期表的发现
1869年俄国化学门捷列夫对当时已知的63种元素进行了规律性的分类。他把每种元素的名称、化学式(将在课题4学习)、相对原子质量、物理性质、化学性质以及主要化合物都写在卡片上,并将所有卡片进行系列组合。门捷列夫激动地发现每一行元素的性质都是按照相对原子质量的增大而逐渐变化着,由此他根据元素的相对原子质量及化学性质的相似性试着将63种化学元素列成表,并在表格中留出空位,预测了一些尚未发现的元素的存在。若干年后科学家们通过一系列实验发现了镓、钪、锗等元素的存在,证实了门捷列夫元素周期表的科学性。门捷列夫工作的成功,引起了科学界的震动,人们为了纪念他的功绩,就把元素周期表称为门捷列夫元素周期表。
四、核外电子的排布
1.核外电子的分层排布
在含有多电子的原子里,核外电子离核远近是不同的,为了形象地说明运动着的电子离核远近的不同,我们引入电子层的概念,这样就可以形象地认为电子是在不同的电子层上运动的,它们的运动是有一定的规律。它不像行星绕太阳旋转有固定的轨道,但有经常出现的区域。
(1)在含多电子的原子里,电子的能量不同。能量低的,通常在离核近的区域运动。能量高的,通常在离核远的区域运动。
(2)通常就用电子层来表明运动着的电子离核远近的不同。
(3)把能量最低、离核最近的叫第一层,能量稍高、离核稍远的叫第二层,由里往外依次类推,叫三、四、五、六、七层。从第一层到第七层的符号分别为:K、L、M、N、O、P、Q。
(4)电子从离核最进的电子层(K层)开始排,K层排满后开始排L层,从里向外依次排布。
(5)每个电子层最多能够容纳的电子数是2n2个(K层,n=1,最多排2个;L层,n=2,最多排8个,依此类推)。
(6)最外层不超过8个电子(K层为最外层时,最多排2个电子)。
按照上述排布规律,我们能够将1~18号元素的核外电子排布情况画出来。对于20号以后的元素核外电子排布情况复杂,暂时不讨论。
2.原子结构示意图的画法:
画圆圈标核电荷数、正号写在前,弧线呈扇面,数字一条线。其中,圆圈代表原子核,弧线代表电子层,在每条弧线的中部标出该层的电子数。
1~18号元素的原子结构示意图如下:
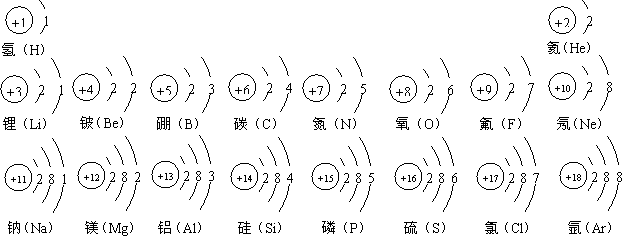
3.元素的性质与原子结构(最外层电子数)的关系
元素的性质,特别是化学性质跟它的原子的最外层电子数目关系非常密切。
(1)稀有气体元素:最外层电子数为8个(氦为2个)电子的结构,性质稳定。因此,稀有气体元素具有稳定结构。稳定结构:最外层为8个电子(K层为最外层,2个电子稳定)。
(2)金属元素:最外层电子数一般少于4个,易失去最外层电子,达到稳定结构。
(3)非金属元素:最外层电子数一般多于或等于4个,最外层易得电子,达到稳定结构。
五、离子的形成
氯化钠的形成过程:
钠原子的最外层只有一个电子,要达到稳定结构需要失去最外层的一个电子;氯原子的最外层有7个电子,要达到稳定结构需要得到一个电子。钠原子的最外层的一个电子向氯原子的最外层上转移,从而使二者的最外电子层都达到稳定结构。Na原子、Cl原子分别失电子、得电子后将带上不同性质的电荷,它们已经从量变引起了质变,分别叫做钠离子(Na+)和氯离子(Cl-)。氯化钠(NaCl)就是由钠离子和氯离子构成的。
类似这样,得、失电子后的原子都带有电荷,不能再称之为原子,而叫离子。某些原子团往往也带有电荷,如SO42-、OH-、NH4+等,它们也叫离子。
1.离子:
带有电荷的原子或原子团叫做离子。
2.分类:
阳离子:带正电,核内质子数大于核外电子数;
阴离子:带负电,核内质子数小于核外电子数。
3.离子符号
用来表示离子的化学符号。离子符号表示式Xn+或Xn-,X表示元素符号或原子团的化学式,X右上角的“+”或“-”表示离子带的是正电荷还是负电荷,“n”表示带n个单位的电荷。例如,Al3+表示1个带3个单位正电荷的铝离子;3SO42-表示3个带两个单位负电荷的硫酸根离子。
4.离子的写法
方法:先写出元素符号,再在右上角标明该离子带的电荷数,注意“+、-”于数字后面。
例:3个硫酸根离子:3SO42-;两个镁离子:2Mg2+
5.离子构成物质
离子和分子、原子一样,都是构成物质的基本粒子。许多物质都是由离子构成的,如:NaCl、KCl、Na2O、CaO、KNO3等。
【例题解析】
A.元素是具有相同核电荷数的微粒 B.元素是具有相同电子数的微粒
C.元素是具有相同中子数的一类原子 D.元素是具有相同质子数的一类原子的总称
【分析】本题考查对于元素的概念的理解。元素就是具有相同核电荷数(即核内质子数)的一类原子的总称。根据定义,D是正确的。B选项中,电子数经常会随着化学反应的发生改变,而电子的得失并不改变质子数,因此虽然在原子中质子数与核外电子数相等,但在元素定义中不可用核外电子数来判断元素种类。C选项,同种元素的原子的中子数不一定完全相同。如碳元素有碳12原子(6个质子、6个中子),也有碳13原子(6个质子、7个中子)和碳14原子(6个质子、8个中子),这3种碳原子的中子数都不相同,但都属于碳元素。A选项,元素是一个宏观、抽象的概念,元素不可能以微粒为定义的中心词。
本题答案:D
A.若两种粒子的核外电子数相同,这两种粒子一定是同种元素
B.若两种粒子的质子数相同,这两种粒子一定是同种元素
C.若两种粒子只含一种元素,则这两种粒子的原子核中质子数一定相同
D.若两种粒子是同种元素,这两种粒子的最外层电子数一定相同
【分析】本题是对粒子的结构与元素之间的关系的辨析。A选项,核外电子数相同不一定是同种元素,如钠离子和氖原子,核外电子总数都是10,但不属于同种元素。B选项,没有确定粒子的种类,不能确定这两种粒子是同种元素,如H2分子 和He原子的质子数都是2,但不是同种元素。C选项,规定了两种粒子只含一种元素,则这两种粒子属于同种元素,则原子核中的质子数相同,因此C是正确的。D选项,同种元素的最外层电子数不一定相同,如钠原子和钠离子,最外层电子数前者是1,后者是8。
本题答案:C
A. 23,53 B.26,30 C.26,56 D.23,46
【分析】本题考查离子的核外电子数和质子数之间的关系。A3+离子带3个正电荷,核外电子数为23,则核内质子数为23+3=26。相对原子质量等于质子数与中子数之和,故M的相对原子质量为26+30=56。
本题答案:C
A.最外层电子数为8的微粒都是稀有气体元素的原子。
B.质子总数和核外电子总数都相同的微粒,一定是同种微粒。
C.氯原子和氯离子属于同种元素,具有相同的电子层数。
D.镁离子与氧离子的核外电子层结构不同。
【分析】本题考查核外电子的排布、最外层电子数和元素种类之间的关系。A.氦元素的原子最外层电子数为2,氦元素也属于稀有气体元素。B.选项中提出的是微粒,微粒包括分子、原子、离子等,本项可以是H2O分子和He原子相比较,它们的质子总数都是10,核外电子总数也是10,但它们显然不是同种微粒。C.质子数相同即为同种元素,画出原子、离子结构示意图就可以判断氯原子和氯离子都有3层电子,是正确选项。D.镁离子和氧离子都是有两层电子。同学们要养成随手画出原子、离子结构示意图的习惯,帮助思考就能保证这类题目的正确率。
本题答案:C
(1)写出下列符号:A原子_________,B的阴离子_________。
(2)C原子结构示意图_________,D离子结构示意图_________。
(3)E属于_________元素(填元素分类)。
【分析】A元素的原子核有一个质子,质子数等于原子序数,可知该元素是氢元素,元素符号为H。B元素的阴离子与氩原子电子层结构相同,即B的阴离子核外电子总数是18,因为带一个单位负电荷,所以质子数为17,即氯离子,离子符号为Cl-。C元素的最外层是第二层,电子数是次外层的2倍,次外层即第一层可排2个电子,因此第2层排了4个电子。质子数为6。D元素的原子比C元素的原子多一个电子层即有3层,该原子要形成阳离子失去1个电子后排满两层共10个电子,则D元素的原子为11个质子的钠原子,钠离子结构示意图见答案。E,地壳中含量最多的元素是氧元素,属于非金属元素。
本题答案:(1)H,Cl-。 (2)
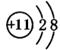 (3)非金属
(3)非金属
