从组成上区分纯净物和混合物、单质和化合物、有机物和无机物。用粒子的观点解释某些常见的现象。
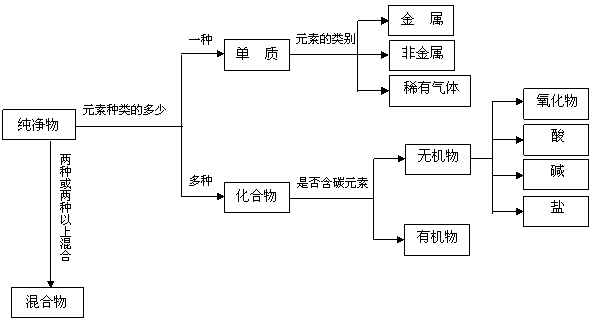
(二) 微粒构成物质
宏观物质都是由微观粒子构成的。
1.分子、原子、离子都是构成物质的粒子,它们之间的关系如下:

2.原子的构成

(1) 质子数=核电荷数=原子序数=核外电子数,原子不显电性。
(2) 质子数+中子数=相对原子质量(数值),原子的质量主要集中在原子核上。
(3) 不是所有原子的原子核都有中子。
(4) 核外电子是分层排布的(认识原子结构示意图)。
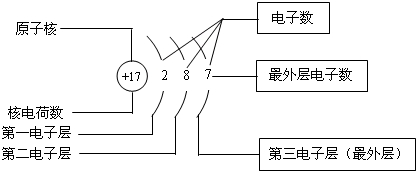
3.分子和原子、离子与原子的本质区别
(1) 分子的定义:分子是保持物质化学性质的最小粒子。
提示:分子在物理变化中不可分,分子间的距离可变化;分子在化学变化中可分,分子中的原子可重新组合,构成新的分子。
原子的定义:原子是化学变化中的最小粒子。
提示:原子在化学变化中不可分,但原子可重新组合。
(2) 认识分子的主要性质,并能用分子的性质解释一些基本问题。
a.分子的体积和质量都很小
b.分子总是在不停地运动
c.分子间有一定的间隙
d.分子在化学变化中可分
(三)化学元素
1.定义:元素是具有相同核电荷数(即核内质子数)的一类原子的总称。
已经发现的元素有一百余种。地壳里和生命细胞中含量最多的元素是氧。地壳里含量较多的元素还有:硅、铝、铁、钙、钠、钾、镁等;生命细胞中含量较多的元素还有:碳、氢、氮、钙、磷等。
2.两个决定:在原子结构中,核内质子数决定元素的种类;
最外层电子数主要决定元素的化学性质。
3.元素的简单分类:金属元素、非金属元素和稀有气体元素。
| 元素的简单分类 | 最外层电子数 | 化学性质 |
| 金属元素 | 一般为1~3个 | 较易失电子形成阳离子 |
| 非金属元素 | 一般为5~7个 | 较易得电子形成阴离子 |
| 稀有气体元素 | 8个(氦为2个) | 化学性质稳定 |
5.提示:元素只论种类,不论个数。
(四)物质组成的表示
1.物质的构成
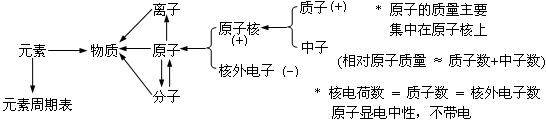
2.物质组成的表示
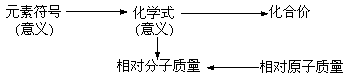
3.化学式:表示物质的组成。
纯净物的组成是固定不变的,一种物质只有一个化学式。
4.化学式与化合价的关系
根据化学式可以推算化合价,根据化合价可以书写化学式。
(1)在单质里,元素的化合价为零。
(2)在化合物里,正负化合价的代数和为零。
5.化学式的涵义(以H2O为例)
可以从宏观和微观来理解它的涵义。
宏观:(1)表示水这种物质。
(2)表示水是由氢元素和氧元素组成的。
(3)表示水中氢元素和氧元素的质量比为1:8。
微观:(1)表示一个水分子。
(2)表示水是由大量的水分子构成的。
(3)表示一个水分子是由两个氢原子和一个氧原子构成的。
(五)溶液
1.溶液知识体系

2.几个概念
溶液:一种或几种物质分散到另一种物质里,形成的均一的、稳定的混合物叫做溶液。
溶剂:能溶解其他物质的物质叫溶剂。
溶质:被溶解的物质叫做溶质。
最常用的溶剂是水,汽油、乙醇等也可以做溶剂。如碘酒,碘是溶质,酒精是溶剂。溶质可以是固体,也可以是液体或气体。如果两种液体互相溶解时,一般把量多的一种叫做溶剂,量少的一种叫做溶质。如果其中有一种是水,一般把水叫做溶剂。
3.溶液的基本特征:均一性和稳定性。
4.溶液中,溶液的质量=溶质的质量+溶剂的质量
5.在溶解过程中发生了两种变化,一种是溶质的分子(或离子)向水中扩散,这一过程吸收热量;另一种是溶质的分子(或离子)和水分子作用,生成水合分子(或水合离子),这一过程放出热量。
即:扩散──吸热; 水合──放热。
当Q吸>Q放:水溶液的温度降低;NH4NO3溶于水时吸收热量;
当Q吸<Q放:水溶液的温度升高;NaOH、浓硫酸等溶于时放出热量;
当Q吸=Q放:水溶液的温度不变。NaCl溶于水溶液的温度变化不大。
6.饱和溶液和不饱和溶液
在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得的溶液叫做饱和溶液,还能继续溶解的溶液叫做不饱和溶液。
不饱和溶液与饱和溶液间的相互转化:
7.溶解度的概念:在一定温度下,某固态物质在100 g溶剂(通常溶剂为水)里达到饱和状态时所溶解的质量。
(1)“易溶”、“可溶”、“微溶”、“难溶”等表示的意思:
| 溶解度/g | >10 | 1~10 | 0.01~1 | <0.01 |
| 溶解性 | 易溶 | 可溶 | 微溶 | 难溶 |
用纵坐标表示溶解度,横坐标表示温度,绘制出的溶解度随温度而变化的曲线叫做溶解度曲线。
溶解度曲线表示的有关信息:
①某物质在某温度时的溶解度;
②同一物质在不同温度时的溶解度是不同的;
③不同物质在同一温度时的溶解度可能不同;
④曲线的交点所表示某一温度下不同物质的溶解度相同。
⑤物质的溶解度受温度影响的变化;
……
(3)气体的溶解度
气体的溶解度是指在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。一般情况下,气体的溶解度随外界压强的增大而增大;随温度的升高而降低。
气体溶解度在实际测定时比较复杂,非标准状况下的数据还应该换算成标准状况下的值。
8.溶质的质量分数
溶质质量=溶液质量×溶质的质量分数
溶剂质量=溶液质量-溶质质量
【例题解析】

分析:本题考查物质的分类。A选项是自来水,属于混合物;B选项C70,一种碳的单质,故属于纯净物;C选项石灰石,是混合物,主要成分是碳酸钙。D选项石油是混合物。
本题答案:B
A.可能是单质或化合物
B.可能是纯净物或混合物
C.一定是纯净物
D.一定是一种单质
【解析】单质是由同种元素组成的纯净物,化合物是由不同种元素组成的纯净物。混合物是两种或多种物质组成的,纯净物只含一种物质。要判断一种物质是单质或化合物,前提条件是该物质必须是纯净物,而题中某物质只含一种元素,而不是一种物质,由此不能确定是纯净物还是混合物,因为混合物也可能只含一种元素,如金刚石和石墨组成的混合物只含碳元素。若该物质是纯净物,则一定是一种单质,故可能是单质正确,但不可能是化合物,因化合物中至少含有两种元素。
【解答】 B
(1)构成物质的基本微粒是_________________________。
(2)构成原子的基本微粒是_________________________。
(3)显示电中性的微粒有_________________________。
(4)质量最小的微粒是_________________________。
(5)参加化学反应一定发生变化的微粒是_________________________。
(6)原子中数目一定相等的微粒是_________________________。
【解析】利用上述微粒的结构、性质等来回答。
【答案】(1)分子、原子、离子; (2)质子、中子、电子; (3)中子、分子、原子; (4)电子; (5)分子; (6)质子和电子。
