能跟酸或碱的溶液起作用而显示不同颜色的试剂叫做酸碱指示剂,通常也简称指示剂。常见的酸碱指示剂有石蕊和酚酞溶液。
石蕊溶液遇酸溶液变成红色,遇碱溶液变成蓝色;酚酞溶液遇酸溶液不变色,遇碱溶液变成红色。
| 加入紫色石蕊试液颜色变化 | 加入无色酚酞试液颜色变化 | |
| 白醋 | 红色 | 不变色 |
| 石灰水 | 蓝色 | 红色 |
| 稀盐酸 | 红色 | 不变色 |
| 氢氧化钠溶液 | 蓝色 | 红色 |
二、常见的酸
1、观察盐酸、硫酸等酸的颜色状态等物理性质
酸的物理性质可用概括性的字表达,如“色、态、味、沸点、密度等”:
盐酸是无色液体,浓盐酸打开瓶盖后,在瓶口产生白雾,这是挥发出来的氯化氢气体与空气中的水蒸气形成盐酸小液滴的缘故。
纯硫酸是一种无色油状液体,难挥发,易溶于水,能以任意比与水混溶。硫酸的密度比水大。沸点高,难挥发。
酸都有腐蚀性,是危险品,使用时一定要注意安全。
2、介绍酸的用途
盐酸是重要的化工产品,可以用于金属表面除锈、制造药物等,人体胃液中含有盐酸,可以帮助消化。
硫酸是重要的基本化工产品之一。可用于制造化肥、农药、火药、燃料以及冶炼金属、金属除锈等。掌握它的性质可以更好地认识它在工农业生产和国防上的重要用途。
三、盐酸、硫酸等酸的化学性质
通性:
⑴酸与指示剂的作用
酸能使紫色石蕊溶液变成红色,遇无色酚酞溶液不变色。类比迁移方法——盐酸、硫酸使石蕊溶液变红,则硝酸、醋酸、苹果汁、桔子汁都能使石蕊溶液变红。
⑵酸与活泼金属的反应
酸与金属活动顺序表中H以前的金属反应,越靠前的金属与酸反应越剧烈,但不是所有的金属都可与酸发生反应。
Mg+2HCl=MgCl2+H2↑ Zn+2HCl=ZnCl2+H2↑
Fe+2HCl=FeCl2+H2↑
注意:①浓硫酸和硝酸与金属反应不产生氢气;
②浓盐酸挥发性强,生成的氢气中会混有大量氯化氢气体。
⑶酸与金属氧化物的反应
酸能与一些金属氧化物反应。我们可以利用这一性质除锈。将一根生锈的铁钉分别放入盛有稀硫酸或稀盐酸的试管中,可以观察到铁锈逐渐消失,溶液由无色慢慢变成黄色。
Fe2O3 + 6HCl=2FeCl3 + 3H2O Fe2O3 + 3H2SO4=Fe2(SO4)3 + 3H2O
但要注意不能把金属制品长时间的浸入酸中,否则金属也会与酸反应而腐蚀掉。当酸不足或适量时,铁锈与酸反应;当酸过量时,与铁锈反应剩余的酸就会继续与铁反应。可以观察到开始时铁锈逐渐消失,溶液由无色慢慢变成黄色,当铁锈消失以后,铁钉表面会冒出无色气泡,溶液颜色变淡,最后由黄色变成浅绿色:
Fe+2HCl=FeCl2+H2↑
⑷酸和碱的中和反应
酸和碱反应,生成盐和水。
如:NaOH + HCl = NaCl + H2O
2NaOH + H2SO4 = Na2SO4 + 2H2O
Ca(OH)2 + 2HCl = CaCl2 + 2H2O
Ca(OH)2 + H2SO4 = CaSO4 + 2H2O
中和反应:酸与碱作用生成盐和水的反应。
⑸酸和盐的反应
酸和盐反应,生成新盐和新酸。
如:Na2CO3+2HCl=2NaCl+H2O+CO2↑
酸的性质实验探究报告可简单总结如下:
| 猜想和假设 | 实验方法 | 现 象 | 结论(或化学方程式) |
| 1.酸使紫色石蕊溶液变色。 | 分别取稀盐酸、稀硫酸1 mL~2 mL于试管中,滴入1~2滴紫色石蕊溶液。 | 变红色。 | 酸使紫色石蕊溶液变红色。 |
| 2.酸使无色酚酞溶液变色。 | 分别取稀盐酸、稀硫酸1 mL~2 mL于试管中,滴入1~2滴无色酚酞溶液。 | 不变色。 | 酸不使无色酚酞溶液变色。 |
| 3.酸与铁钉反应。 | 取光亮的铁钉于试管中,再加入稀盐酸或稀硫酸浸没铁钉。 | 铁钉表面有气泡,溶液由无色变浅绿色。 | Fe+2HCl=FeCl2+H2↑ |
| 4.酸与氢氧化钠溶液反应。 | 取1 mL~2 mL氢氧化钠溶液于试管中,滴入1~2滴无色酚酞溶液,再滴加稀盐酸或稀硫酸。 | 溶液由无色→红色→无色 | NaOH+HCl=NaCl+H2O 2NaOH+H2SO4=Na2SO4+2H2O |
| 5.酸与铁锈反应。 | 取带锈的铁钉于试管中,再加入稀盐酸或稀硫酸浸没铁钉,然后加热。 | 铁锈逐渐消失,溶液由无色→黄色,铁钉表面有气泡。 | Fe2O3+6HCl=2FeCl3+3H2O Fe2O3+3H2SO4=Fe2(SO4)3+3H2O Fe+2HCl=FeCl2+H2↑ Fe+H2SO4=FeSO4+H2↑ |
| 6.酸与碳酸钠溶液反应。 | 取1 mL~2 mL碳酸钠溶液于试管中,滴加稀盐酸。 | 有气泡。 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
四、浓硫酸的特殊性质
1、腐蚀性——脱水性
浓硫酸有强烈的腐蚀性,用时一定要注意安全。我们做实验时不掌握好浓硫酸的这一“个性”,很可能就被腐蚀皮肤、衣服等。浓硫酸的腐蚀性原因本质上是它的脱水性造成的,它能将纸张、木材、布料、皮肤等物质中的氢、氧元素按水的组成比脱去,生成黑色的碳。所以,使用浓硫酸时要特别小心。不慎将浓硫酸沾到皮肤或衣服上后的正确处理方法:立即用大量水冲洗,之后涂上3%~5%的NaHCO3溶液,对于皮肤还要尽快到医院治疗。
2、吸水性——干燥剂
浓硫酸具有吸水性,可以做干燥剂。与脱水性不同的是,吸水性表现为可以直接吸收空气或其它气体中本来就存在的水分子。此时浓硫酸溶质不变,溶剂增加,溶质的质量分数降低。浓硫酸可以干燥初中常见的气体,但是不可以干燥氨气。
3、浓硫酸的稀释
在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢的注入水中,并不断的搅拌。切不可将水倒进浓硫酸里,这样会引起水沸腾携带酸液爆溅。稀释浓硫酸不正确操作的后果:导致伤人或腐蚀物品。
例题分析
稀盐酸可以使石蕊溶液变红。我们已经知道,在稀盐酸中存在有H2O、Cl-和H+等粒子。请你设计几个简单实验,探究可能是稀盐酸中的哪一种粒子使石蕊溶液变红(写出简要的实验步骤、观察到的现象以及由此得到的结论)。
解析:
方法一:用两支试管分别取少量蒸馏水和 NaCl溶液,各滴加紫色石蕊溶液,均不变红,说明 H2O分子和 Cl-均不能使石蕊变红。说明盐酸中的H+使石蕊变红。
方法二:用试管取少量稀盐酸,滴加紫色石蕊溶液,溶液变红。逐滴加入NaOH溶液,试管中的溶液由红色变紫,最后变成蓝色。在反应后的溶液中,H2O分子和Cl-离子仍然存在,而H+离子全部生成H2O分子。说明H2O分子和Cl-离子都不能使石蕊变红,是稀盐酸中的H+使石蕊变红。
资料介绍
一、自制指示剂
实验原理
许多植物的花、果、茎、叶中都含有色素,这些色素在酸性溶液或碱性溶液里显示不同的颜色,可以作为酸碱指示剂。
实验用品
玻璃杯、研钵(或榨汁机)、纱布。
花瓣(如牵牛花)、植物叶子(如紫甘蓝)、萝卜(如胡萝卜、北京心里美萝卜)、酒精溶液(乙醇与水的体积比为1∶1)。
实验步骤
取一些花瓣、植物叶子、萝卜等,分别在研钵中捣烂后,各加入适量酒精溶液,搅拌浸泡。半小时后,再分别用四层纱布将浸泡出的汁过滤或挤出,就得到指示剂。将自制的指示剂分别装入小瓶中,并贴上标签备用。
二、酸碱指示剂的发现
英国著名化学家、近代化学的奠基人罗伯特·波义耳(Robert Boyle,1627~1691)在一次实验中,不小心将浓盐酸溅到一束紫罗兰上,为了洗掉花瓣上的酸,他把花浸泡在水中。过一会儿,他惊奇地发现紫罗兰变成红色。 他请助手把紫罗兰花瓣分成小片投到其他的酸溶液中,结果花瓣都变成了红色。波义耳敏锐地觉察到,把紫罗兰花瓣投进一种溶液中,就能确定这种溶液是否显酸性。波义耳从各种花和一些植物中提取汁液,并用它制成了试纸。波义耳用试纸对酸性溶液和碱性溶液进行多次试验,终于发现了我们今天还在使用的酸碱指示剂。
【例题解析】
A.没有特殊要求
B.把浓硫酸沿器壁慢慢地注入水中,并不断搅动
C.把水缓缓地倒入浓硫酸中,并不断搅动
D.迅速将浓硫酸倒入水中后搅动
【分析】 浓硫酸溶于水时会放出大量的热。因此在稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢地注入水中,并不断搅动,使产生的热量迅速地扩散,切不可把水倒进浓硫酸里。
答案:B
(1)①②与③④分别根据物质的_________________、______________性质来作判断。
(2)你认为③④两个实验是根据酸类的哪些性质设计的?
________________________________________________________________。
(3)产生的气体物质从分类看,它们的区别________________、__________________。
【分析】 本题考查分别利用醋酸的物理性质和化学性质进行物质的检验。①②是利用醋酸的物理性质,通过嗅觉和味觉进行检验;③④是利用醋酸与碳酸盐(纯碱)和活泼金属(铁)的化学反应,通过特征现象进行检验;反应中产生的气体分别为CO2、H2,从物质的分类角度来看,分别属于化合物和单质。
答案:
(1)物理、化学
(2)酸能和某些盐反应,酸能和较活泼金属反应
(3)产生的二氧化碳是化合物(氧化物),产生的氢气是单质(非金属单质)。
 究活动。
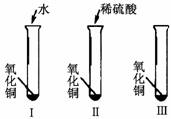
究活动。(1)你提出的假设是___________________________________;
(2)通过实验Ⅰ可以证明_______________________________;
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和实验Ⅲ,在实验Ⅲ中应该加入____________;
(4)实验结果为____________。
【分析】 本题以硫酸与CuO反应为素材,通过设计对比实验探究稀硫酸能使氧化铜溶解的粒子,考查了化学实验的方案设计和原理探究的能力。即分别将H2O、H+、SO42-三种粒子设计在三支试管中分别与CuO接触,通过对比观察实验现象探究稀硫酸中能使氧化铜溶解的粒子。难点在第三小题,实验设计重在利用“对比”的方法,要研究氢离子,可以找一种有氢离子,但所含阴离子的不同的物质如盐酸;要研究硫酸根离子,可以找一种含硫酸根离子,但所含氧离子不同的物质如硫酸钠即可。
答案:
(1) 溶液中H+使CuO溶解。
(2) H2O不能溶解CuO。
(3) 盐酸或硫酸钠溶液。
(4) 溶液中的H+可以使CuO溶解,H2O 、SO42-不能使CuO溶解。
