1、定义
一种或几种物质分散到另一种物质里,形成的均一的、稳定的混合物叫做溶液。
2、溶液的特点
(1)均一性:溶液各部分的性质相同。
(2)稳定性:外界条件不变时,溶液久置,不分层。
3、溶液的组成
溶质溶解在溶剂中形成溶液。能溶解其他物质的物质叫溶剂,被溶解的物质叫做溶质。如食盐水中,食盐是溶质,水是溶剂。
最常用的溶剂是水,汽油、乙醇等也可以做溶剂。如碘酒,碘是溶质,酒精是溶剂。
溶质可以是固体,也可以是液体或气体。如果两种液体互相溶解时,一般把量多的一种叫做溶剂,量少的一种叫做溶质;如果其中有一种是水,一般把水叫做溶剂。
4、说明
(1)不同溶质在同一溶剂里的溶解性不同,同种溶质在不同溶剂里的溶解性也不同。如碘不易溶解在水中而易溶于酒精,高锰酸钾不易溶于汽油而易溶于水。
(2)溶质可以是一种也可以是多种,把一种溶液加入到另一种溶液中也能形成溶液,属于混合溶液。
5、两种重要的量的关系
(1)质量关系
溶液的质量=溶质的质量+溶剂的质量
(2)体积关系
溶液的体积≠溶质的体积+溶剂的体积
6、用途
由于在形成溶液的过程中,构成溶质的微粒均匀的分散在水分子中,提高了反应物之间的接触面积,因此在溶液里进行的化学反应常是比较快的。所以,在实验室里或化工生产中,要使两种能起反应的固体起反应,常常先把它们溶解,然后把两种溶液混合,并加以振荡或搅动,以加快反应的进行。
溶液对动植物的生理活动也有很大意义。动物摄取食物里的养料,必须经过消化,变成溶液,才能吸收。在动物体内氧气和二氧化碳也是溶解在血液中进行循环的。在医疗上用的葡萄糖溶液和生理盐水、医治细菌感染引起的各种炎症的注射液(如庆大霉素、卡那霉素)、各种眼药水等,都是按一定的要求配成溶液使用的。植物从土壤里获得各种养料,也要成为溶液,才能由根部吸收。土壤里含有水分,里面溶解了多种物质,形成土壤溶液,土壤溶液里就含有植物需要的养料。许多肥料,像人粪尿、牛马粪、农作物秸秆、野草,等等,在施用以前都要经过腐熟的过程,目的之一是使复杂的难溶的有机物变成简单的易溶的物质,这些物质能溶解在土壤溶液里,供农作物吸收。
二、乳浊液
1、定义
小液滴分散到液体里形成的混合物叫做乳浊液。
2、特点
乳浊液不均一,也不稳定,静置后会出现分层现象。
3、示例
植物油加入水中、汽油与水混合等。
4、乳化作用
两种互不相溶的液体,加入乳化剂时,能够形成一种比较稳定的乳浊液。在生活中时常遇到“乳化”现象,“乳化”并不是溶解,只是使小液滴分散成无数细小的液滴存在于水中,而不聚集成大的液滴,这与物质溶解在水中是完全不同的。利用这个原理,可以用加入洗涤剂的水洗去衣服、餐具上的油污。洗洁精、洗衣粉等含表面活性剂的物质可以使食用油等物质以细小的液滴形式均匀分散在水中形成乳浊液,这种作用称为乳化作用。
注意:汽油去除衣服上的油漆利用的不是乳化作用,而是汽油溶解了油漆。
三、悬浊液
1、定义
固体颗粒分散到液体中形成的混合物叫做悬浊液。
2、特点
悬浊液不均一,也不稳定,静置后会出现分层现象。
3、示例
泥浆水、少量二氧化碳通入澄清的石灰水等。
四、溶解时的吸热或放热现象
1、典型物质溶于水的温度变化
NaOH溶于水,溶液温度升高;
NH4NO3溶于水,溶液温度降低;
NaCl溶于水,溶液温度无明显变化。
2、原因分析
在溶解过程中发生了两种变化,一种是溶质的分子(或离子)向水中扩散,即扩散过程,这一过程吸收热量;另一种是溶质的分子(或离子)和水分子作用,生成水合分子(或水合离子),即水合过程,这一过程放出热量。
即:扩散──吸热;水合──放热。
扩散过程吸收的热量 > 水合过程放出的热量,温度降低,如: NH4NO3溶于水。
扩散过程吸收的热量 < 水合过程放出的热量,温度升高,如: NaOH溶于水。
扩散过程吸收的热量 ≈ 水合过程放出的热量,温度无明显变化,如: NaCl溶于水。
3、可以设计实验方案,探究物质溶于水时是放出热量还是吸收热量。这可以培养大家的思维发散性和创新性。同时,对设计的实验方案可以进行分类,使思维条理化。
(1)敞口体系
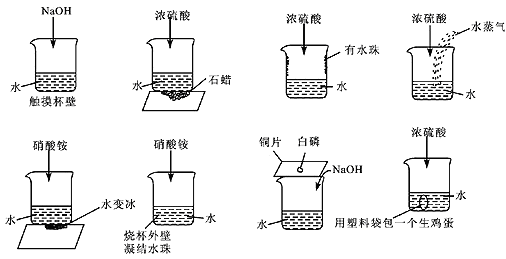
(2)封闭体系
封闭一定量的气体,观察由于物质的溶解产生的热量变化对气体压强带来的影响而产生的现象。
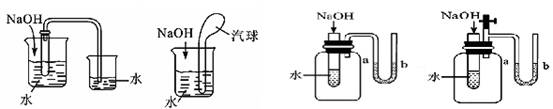
五、饱和溶液和不饱和溶液
1、定义
在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得的溶液叫做饱和溶液,还能继续溶解的溶液叫做不饱和溶液。
饱和溶液定义要点:“一定温度下”“一定量的溶剂”。
2、不饱和溶液与饱和溶液间的相互转化:
饱和溶液的判断方法:
判断某溶液是否饱和的方法就是其他条件不变,加入溶质看能否继续溶解该溶质。
附加:生活中的化学(去掉油漆、油墨等油渍妙法)
(1)油漆渍:新沾上的油漆可用松节油、香蕉水、苯四氯化碳等溶剂擦除。陈渍可将污处浸在10~20%的氨水或硼砂溶液中使油漆溶解去除。将污处浸入1:1的乙醚和松节油的混合液中,把污渍浸软,然后用汽油擦拭,效果也很好。
(2)油墨渍:用汽油、松节油、四氯化碳浸泡或揩擦,然后用水漂洗即可去除。
(3)皮鞋油渍:用汽油润湿,然后用10%的氨水清洗,再用酒精揩拭。
(4)印泥油渍:和温热皂液浸10分钟后搓洗,再用95%的酒精擦洗。
(5)万能胶渍:将丙酮或香蕉水滴在斑迹上,然后用刷子将斑迹刷软,再用清水洗净。
(6)蜡笔和复写纸渍:先在温洗衣粉溶液中洗,然后用汽油擦拭,最后用酒精擦净即可。
(7)牛奶渍:一般用冷水就可洗掉,也可用汽油或丙酮擦除。不易去掉的,可用棉花或蘸过氧化氢溶液擦除,然后用水洗净。也可用洗涤剂洗后,再用淡氨水洗。
(8)柿子渍:立即用葡萄酒加浓盐水揉搓,再用温洗涤洗液清洗,最后用清水漂净。
(9)水果汁:新渍可用浓盐水揩拭污处,或立即把食盐撒在污处,用手轻搓,再在洗涤剂溶液中洗净。陈渍可先用5%的氨水浸泡,然后再用洗涤剂清洗,用清水漂净。
【例题解析】
A.溶液虽均一稳定,但未必无色
B.溶液中各部分的性质是相同的
C.如果温度不变,水不蒸发,食盐溶液久置也不会分离出食盐晶体
D.一种溶液中只能含一种溶质
【分析】溶液具有以下特征:
(1)各部分的组成性质完全相同,外观看起来均匀、透明、澄清,这一特征为“均一性”。
(2)只要不改变溶液的条件,如温度、压强等,不蒸发水分,溶液长期放置也不会有溶质分离析出,这一特征为“稳定性”。因此,对于题中有关溶液的叙述,很容易判断出B、C是正确的。溶液是均一、透明的,但不一定无色,如CuSO4溶液就是蓝色的,FeCl3溶液是黄色的,由此可判断A也是正确的。一种溶液可同时溶解多种溶质,形成“混合溶液”,如生活中常见的溶液——雪碧等饮料,故D的说法不正确。
答案:D。
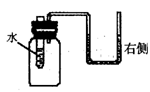 不与水发生化学反应的物质后,原来U型管内两臂处在同一水平面上的红墨水,发现其右侧液面降低了一些,左边的液面上升了一些,你认为所则加入的物质是( )
不与水发生化学反应的物质后,原来U型管内两臂处在同一水平面上的红墨水,发现其右侧液面降低了一些,左边的液面上升了一些,你认为所则加入的物质是( ) A.活性炭 B.生石灰 C.硝酸铵 D.苛性钠
【分析】U型管中红墨水呈左边高、右边低的状况,说明广口瓶内气体的压强增大,大于大气压,导致这种现象的原因是在试管中的水里加入某种物质因溶解而吸热,造成温度降低,从而引起气体压强减小。因此,应选择C选项,因为硝酸铵在溶解于水时,其扩散过程吸收的热量大于水合过程放出的热量。B、C在溶于水的过程中能使溶液的温度升高,会引起U型管中红墨水呈左边低。右边高的状况。活性炭加入水中不能溶解,无明显热量变化,也不会造成红墨水液面的升降。
答案:C。
(1) CuSO4溶液
(2) 盐酸
(3) 碘酒
(4) 10 mL酒精和20 mL汽油的混合物
(5) 10 mL水和20 mL酒精的混合物
【分析】本题考查溶液中溶质和溶剂的确定。当固体溶于液体时,固体是溶质,液体是溶剂,如;如果两种液体互相溶解时,一般把量多的一种叫做溶剂,量少的一种叫做溶质,如(4)酒精体积小为溶质,汽油体积大为溶剂;如果其中有一种是水,一般把水叫做溶剂,如(5)有水则水为溶剂。
答案:
(1)溶质是CuSO4,溶剂是水;
(2)溶质是HCl气体,溶剂是水;
(3)溶质是碘,溶剂是酒精;
(4)溶质是酒精,溶剂是汽油;
(5)溶质是酒精,溶剂是水。
A.厨房洗涤剂可使餐具上的油污乳化
B.汽油可溶解衣服上的油渍
C.食醋可用来除去热水瓶中的水垢
D.自来水可溶解掉铁栅栏上的铁锈
【分析】洗涤离不开溶剂、溶液、乳浊液,本题所考查的正是这些物质的使用是否恰当的问题。生活经验告诉我们,餐具上的油污是完全可以用厨房洗涤剂(乳餐洗净)来洗掉的,其道理就在于这些洗涤剂能使油污分散成细小的液滴(一种乳浊液),这些细小的液滴可随水流走;汽油作为一种有机溶剂,能溶解许多的有机物,衣服上的油渍就完全可以溶解在汽油中而被除掉;食醋的主要成分是醋酸,能和热水瓶中的水垢(主要成分是碳酸钙、氢氧化镁)发生化学反应,从而形成能溶于水的物质而被除去;铁栅栏上的铁锈成分主要是氧化铁,由于它不溶于水,因此用自来水是不可能将铁锈溶解掉的,这样做,只能进一步加快铁栅栏的锈蚀。
答案:D。
【分析】结晶水合物溶于水后,溶质是化学式的前半部分,结晶水溶于水中作为溶剂的一部分。故CuSO4·5H2O溶于水,溶质是CuSO4,溶剂是水。溶质的质量等于25 g CuSO4·5H2O中CuSO4的质量,溶剂的质量等于25 g CuSO4·5H2O中结晶水的质量加上200 g水的质量。
答案:溶质的质量=16 g,溶剂的质量=209 g。
A. 饱和溶液就是不能继续溶解溶质的溶液
B. 同一溶质的饱和溶液一定比不饱和溶液浓
C.饱和溶液不会变成不饱和溶液,不饱和溶液也不会变成饱和溶液
D. 饱和溶液在一定条件下可转化为不饱和溶液
【分析】此题主要考查“饱和溶液”的概念。在理解这个概念时,要注意如下几个关键:
①一定温度、一定量的溶剂;
②同种溶质溶解的量不能继续增加(但其它溶质可以继续溶解)。比较同种溶质的饱和溶液、不饱和溶液的浓稀,一定要在同温下进行比较。如A中未指明“一定温度”、“一定量的溶剂”,也未指明是不是同种溶质,故不正确。B中未指明“相同温度”,也不正确。饱和溶液与不饱和溶液在一定条件下可以相互转化,故C是错误的。
答案:D
