1.(09朝阳一模)初中化学课上,同学们利用下列实验探究碱的化学性质:
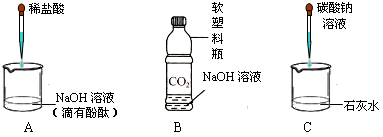
(1)B实验中反应的化学方程式为______________________。
(2)C实验中观察到的现象是__________________________。
(3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞和水外一定含有____________。
老师问:废液中还可能有什么物质?某同学脱口而出:废液中含有氢氧化钠,他的说法正确吗?同学们认为不准确,理由是:____________。于是引发了热烈讨论,下面是大家的发言:
| 学生甲 | 还可能有Ca(OH)2、NaOH | 学生丙 | 还可能有Ca(OH)2、CaCl2 |
| 学生乙 | 还可能有NaOH、Na2CO3 | 学生丁 | 还可能有Na2CO3 |
| …… | ………… |
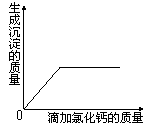
【实验验证】 同学们对可能含有的物质进行确定,取一定
量的废液过滤,向滤液中逐滴加入氯化钙溶液,根据反应
现象绘制了如右图所示的示意图。
【结论解释】 分析图象数据得出可能含有的物质中,
一定含有____________,
一定没有____________,
【拓展提高】那么是否含有氢氧化钠呢?请你帮他继续完成实验,写出探究的实验方法:
______________________________________________________。
2.(09石景山一模)甲、乙两个小组用碳酸钠溶液分别鉴别澄清石灰水与盐酸。实验后将废液倒入各组的烧杯中。
⑴甲组烧杯内废液浑浊,过滤后的滤液中肯定没有上述三种物质中的____________。
⑵乙组烧杯内液体澄清,该组学生对此溶液进行如下探究。
【提出问题】烧杯内澄清溶液中的溶质有什么?
【相关资料】Ⅰ.CaCl2 + Na2CO3 CaCO3↓+ 2NaCl
Ⅱ.CaCl2溶液呈中性
【交流讨论】该小组同学经过仔细分析得出:该溶液中溶质的组成,有以下两种可能,分别是①__________,②__________。
【实验方案设计】请完成下列实验报告。
| 实验操作 | 实验现象 | 实验结论 |
类型二:测定混合物中碳酸钠的质量分数
3.(09东城一模)某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。
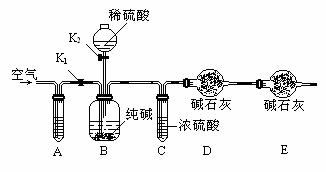
实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为83.4g;
③准确称得6g纯碱样品并放入容器B中;
④关上K1,打开K2,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤关上K2, 打开K1,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g。
试回答:
(1)已知装置A中试剂为碱性溶液,其作用是_____________________。
(2)实验步骤⑤鼓入空气的目的是___________________________。
(3)C装置的作用是 ____________,若没有C装置,则会导致测定结果 __________________(填“偏大”或“偏小”) 。
(4)E装置的作用是____________________。
(5)根据实验中测得的有关数据,计算出纯碱样品碳酸钠的质量分数为_________________%(计算结果保留一位小数)。
(6)经精确测定,样品中碳酸钠的实际质量分数略小于上述所求数值,其原因可能是____________。
4.(08宣武二模)现有甲乙两个小组的学生,欲测定某工业纯碱样品中Na2CO3的质量分数,分别设计并完成实验如下。甲组:取10.00 g样品,向其中加入过量的盐酸,直至样品中无气泡冒出,加热蒸发所得物并在干燥中冷却至室温后称量。反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为10.99 g。
(1) 计算样品中碳酸钠的质量分数____________。(保留一位小数)
(2)实验中能否用稀硫酸替代盐酸,理由是____________。
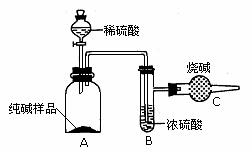
乙组:取10.00 g样品,利用右图所示装置,测出反应后装置C中烧碱增重了3.52 g。
(1)乙组中B装置的作用是____________。
(2)甲组认为乙组不能准确求出样品中碳酸钠的质量分数,建议乙组按下图改进实验,向A装置鼓入空气并增加了D、E装置。请你简述D、E两装置的作用和鼓入空气的目的。
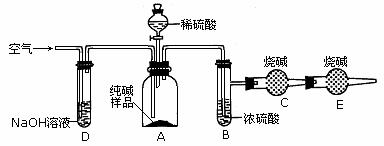
①D装置的作用:____________________________________。
②E装置的作用:____________________________________。
③鼓入空气的目的:_________________________________。
5.(08西城一模)氢氧化钠是一种重要的化工原料,广泛应用于肥皂、石油、造纸、纺织等工业。化工厂的氢氧化钠产品常常含有杂质碳酸钠,为了测定该产品中氢氧化钠的质量分数,某化工厂甲、乙两实验员分别设计了如下实验方案:
(1)甲实验员的方案是:准确称量一定质量的氢氧化钠样品,配制成溶液,加入过量氯化钙溶液,直至沉淀完全,过滤,将所得沉淀洗涤、烘干、称量。
①该反应的化学方程式为________________________。
②过滤后所得滤液中的溶质是____________________(用化学式表示)。
(2)乙实验员的方案如下图所示(假设所取试剂均为足量,且每步反应都充分):
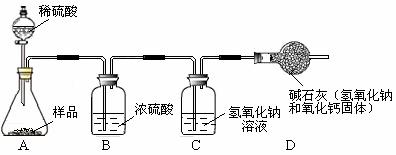
实验中B装置的作用是___________,C装置的作用是_______________,D装置的作用是____________。乙称量实验前后C装置的质量,计算出样品中氢氧化钠的质量分数比实际值偏高。请分析其原因是___________________________________________。
6.(09丰台一模)某校老师让化学实验小组的同学进行有关Na2CO3和NaCl的系列实验。
实验一:鉴别失去标签的Na2CO3溶液和NaCl溶液。
同学们分别选择了下列物质进行实验。其中合理的是 ____________。
①稀盐酸 ②澄清石灰水 ③pH试纸
实验二:除去某NaCl样品中的少量Na2CO3。
同学们设计了如下实验流程图:
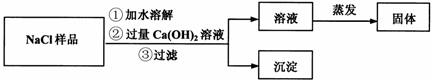
(1)上述流程图中,沉淀的化学式为____________;
(2)实验完毕后,同学们发现溶液中的溶质除含有NaCl外还含有____________。于是同学们改用了新的方案:向样品中滴加稀盐酸至不再产生气体为止。有关反应的化学方程式____________。
实验三:完成了上述实验后,同学们又进行了以下的探究活动。
【实验目的】测定该NaCl样品中Na2CO3的质量分数。
【设计方案】根据实验目的和原理,同学们认为需要测得下列四个数据:
①NaCl样品的质量ag;
②充分反应后,生成沉淀的质量为bg;
③反应前装置和药品的质量为cg;
④充分反应后装置和药品的质量为dg。
【实验用品】老师提供了以下实验用品。
药品:足量的稀H2SO4、CaCl2溶液、碱石灰、浓硫酸
装置:
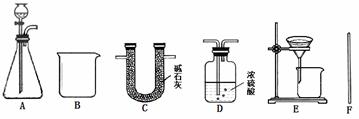
【查阅资料】①CaCl2与Na2CO3两种溶液能发生复分解反应。②碱石灰是烧碱和氧化钙的固体混合物,主要用作气体干燥剂。
【实验报告】请你帮助他们完成下表(碱石灰和浓硫酸已被选用,下表中不再填写)。
| 方案 | 药品 | 实验 装置 |
所需数据 (用ag、bg、cg、dg表示) |
Na2CO3的质量分数计算式 |
| 一 | B、E、F | |||
| 二 | ag、cg、dg | |||
| 三 |
类型三:信息提取类型
7.(08西城一模)小洁发现妈妈在面粉中加入一种白色粉末,做出的蛋糕、馒头疏松多孔。她很感兴趣,想探究这种“神奇粉末”的成分。通过对市场上相关产品进行调查,她发现了如下图所示的三种商品,认为妈妈使用的白色粉末是以下三种商品中的一种。
| 商品 |  |
 | |
| 成分 | 碳酸钠 | 碳酸氢钠 | 碳酸氢钠、有机酸 |
| 用法 | 面粉加水揉和成面团,发酵后产生酸味,加入适量纯碱,反复揉和,加热即可制成松软的馒头。 | 面粉无需发酵,直接加入适量小苏打,加水调和,放入烤箱加热即可制成疏松多孔的糕饼。 | 面粉与发酵粉按比例拌匀,放入适量温水揉和,放置一段时间,即可蒸、烘、烤制成疏松多孔的各种食品。 |
(2)小洁通过阅读纯碱和小苏打的用法,推测出小苏打不同于纯碱的化学性质是
__________________________________________________________________________。
(3)根据获得的信息,小洁设计实验方案,在实验室探究这种白色粉末的成分。
| 实验操作 | 实验现象 | 实验结论 |
| ① 取少量白色粉末于试管中,加入适量蒸馏水。 | 固体溶解,无其他明显现象 | __________________________ |
| ②____________________ | 有无色气泡产生 | 白色粉末一定是纯碱 |
| 实验操作 | 实验现象 | 实验结论 |
8.(09东城一模)某校化学兴趣小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或加热的条件下均不反应。那么,铜与浓硫酸能否发生反应呢?他们设计了如下图所示装置进行探究。
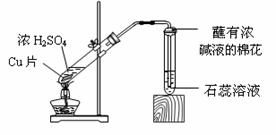
[猜想与假设]
①在常温下能反应 ②常温下不能反应,但在加热条件下能反应
③在加热条件下不能反应
[查阅资料]含有Cu2+的水溶液通常显蓝色
[实验与事实]操作① 将一小块铜片放入试管中,加入足量浓硫酸,无明显现象;
操作② 加热该试管,铜片上有气泡,产生了有刺激性气味的气体;
操作③ 停止加热,将试管中的残液慢慢倒入水中,溶液呈蓝色。
[分析与思考]
⑴甲同学认为,由以上探究可知:猜想____________(填序号)是正确的。
⑵乙同学认为,经检验产生的气体是SO2,所以铜跟浓硫酸在加热条件下反应的产物只是SO2和CuSO4。
⑶丙同学认为,在实验装置中,“蘸有浓碱液棉花”的作用是____________。
[反思与评价]
⑷操作③中,从安全角度考虑____________(填“可以”或“不可以”)将水倒入残液中,其理由是____________。
⑸在[分析与思考]⑵中对产物只是SO2和CuSO4的判断是否准确____________(填“是”或“否”),其理由是____________。
[拓展与应用]
根据以上探究和已掌握的知识,该兴趣小组的同学设计了两个制取硫酸铜的实验方案:
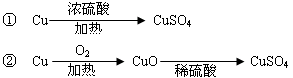
⑹经过对两种方案的讨论、对比,同学们认为方案②具有的优点有____________(填序号),所以工业上制备硫酸铜不是直接利用浓硫酸与铜反应。
A.提高铜的利用率 B.提高硫酸的利用率
C.不产生污染大气的SO2 D.不用浓硫酸,安全性好
9.(08西城二模)草酸的化学式为C2H2O4,甲、乙两位同学对草酸受热分解及其产物的检验做如下探究:
【猜想和假设】(1)草酸分解产物是CO2和H2O;(2)草酸分解产物为CO2和H2;
(3)草酸分解产物为CO2、CO和H2O 。
【查阅资料】(1)碱石灰为NaOH和CaO的固体混合物;
(2)白色的无水硫酸铜遇水变蓝;
(3)草酸晶体熔点较低,加热到182℃时便开始熔化。
【实验设计】甲同学设计了如图1所示的装置,乙同学设计了如图2所示的装置。
(图中铁架台略去)
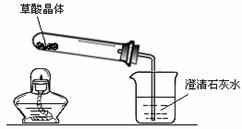
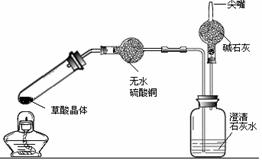
【进行实验】甲同学按图1实验,观察到澄清石灰水变浑浊;乙同学按图2实验,观察到无水硫酸铜由白色变成蓝色,澄清石灰水变浑浊,且生成的气体通过碱石灰后,在尖嘴处能被点燃,在火焰上方罩一个内壁涂有澄清石灰水的烧杯,澄清石灰水变浑浊。
【结论】乙同学证明产物中含有_______________________________________________,
若草酸分解后的产物就是乙同学证明的结果,请写出草酸分解的化学方程式:
__________________________________________________________________________。
【反思与评价】乙同学认为甲同学设计的实验装置有不足之处。甲同学认为乙同学的设计是科学合理的。图2装置优于图1装置有如下几点:
(1)图2中试管口向上倾斜。其原因是___________________________________________;
(2)________________________________________________________________________;
(3)________________________________________________________________________。
乙同学设计的图2装置也能证明产物中无H2,证明方法是________________________________。
10.(07石景山2模)小勇看书得知:潜水艇中常用过氧化钠(Na2O2)作为供给人们呼吸的试剂。
[提出问题] CO2跟Na2O2反应产生的气体是O2吗?
[猜想与假设] CO2跟Na2O2反应产生的气体是O2。
[查阅资料]①Na2O2是一种化学性质活泼的淡黄色颗粒状固体,在通常情况下能分别跟H2O和盐酸等发生化学反应,有O2生成。
②CO2能与Na2CO3水溶液反应生成NaHCO3,CO2在NaHCO3溶液中几乎不溶解;NaHCO3与盐酸反应生成NaCl、H2O和CO2。
[实验探究]小勇设计了如下图所示装置进行探究活动。
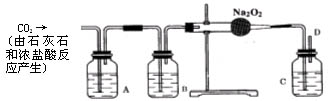
[请你参加]请你参加小明的实验探究活动,回答下列问题。
(1)
| 瓶内液体 | 作用 | 发生反应的化学方程式 | |
| A装置 | |||
| B装置 | |||
| C装置 |
[探究结论]原假设正确。
四、鉴别补充题:
11. 某无色气体可能含有N2、H2、CO、CO2中的一种或几种,将该气体依次通过下列各种药品(假设每一步反应均完全)。

试根据流程图回答问题:
(1)该气体中(填“一定”、“可能”或“肯定不”)__________含有氢气。
(2)写出上述实验中一定能发生反应的化学方程式______________________________________。
(3)根据现象和数据推断原气体的所有可能组成:
_______________________________________________________________________
_______________________________________________________________________
五、实验方案设计与评价:
12.(07石景山)用如右图所示装置干燥并收集某纯净气体,甲、乙、丙三位同学对该气体的组成有不同的认识,请你对他们的推测进行评价:
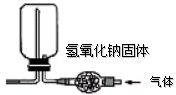
| 推测 | 评价(是否正确,并简述理由) |
| 甲认为可能是O2 | |
| 乙认为可能是CO2 | |
| 丙认为可能是H2 |
