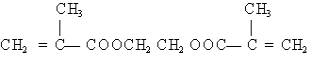| 全国高考理科综合模拟试卷(二十三) | ||||||||||||||||||||||||||||||||||||||||||||
|
(考试时间隔150分钟 满分260分) 可能用到的数据,相对原子量:H—1 C—12 N—14 O—16 Cl—35.5 1—127 Al—27 第Ⅰ卷(选择题,共130分)
一、选择题(每题只有一个选项符合题意,每题3分,共10题,计30分) 1.既能进行有氧呼吸又能进行无氧呼吸,既能进行孢子生殖又能进行出芽生殖的生物有 A.水螅 B.根霉 C.水绵 D.酵母菌 2.把含有生长素的琼脂小块放在幼苗切面端的不同位置上,能正常生长、不发生弯曲的是
3.太阳辐射的能量主要来自太阳内部的 A.裂变反应 B.衰变反应 C.热核反应 D.化学反应 4.下列说法中正确的是 A.光导纤维是利用光的全反射现象 B.雨后天空的彩虹是光的干涉现象 C.根据经典电磁理论可知,原子十分稳定,原子光谱是线状光谱 D.光电效应表明光具有粒子性,从而否定了光的波动性 5.某同学家中有几个用电器:1.5kW电水壶,200W的电冰箱,750W的取暖器,250W的电视机和2kW的空调器,如果进线处所接保险丝的额定电流为13A,供电电压为220WV,则不能同时使用的电器是 A.电水壶和电冰箱 B.取暖器和电冰箱和电水壶 C.电水壶和空调器 D.电冰箱、电视机和空调器 6.下列说法正确是 A.物体在恒力作用下的运动方向是不会改变的 B.加速前进的汽车,后轮所受的摩擦力方向与运动方向相同 C.第一宇宙速度为7.9km/s,因此飞机只有达到7.9km/s才能从地面起飞 D.作用力和反作用力都可以做正功,也都可以做负功 7.下列变化中,不需要破坏化学键的是 A.碘的升华 B.氯化氢气体溶于水 C.石油的裂化 D.加热氯化铵晶体温 8.下列物质的晶体中,不存在小分子的是 A.二氧化碳 B.二氧化硫 C.二氧化氮 D.二氧化硅 9.下列离子方程式书写正确的是 A.氯气与水反应 Cl2+H2O═2H++Cl-+ClO- B.NaOH溶液中通入过量的CO2 CO2 +OH-═HCO3- C.铁跟盐酸反应 2Fe+6H +═2Fe 3++3H2↑ D.碳酸钠跟水反应 CO23 -+H2O═HCO3- +OH- 10.下列有关物质的用途正确的是 ①碘酒可作为医用消毒剂 ②明矾可作为净水剂 ③乙二醇可作为抗冻剂 ④纯净的碳酸钡可作为医用“钡餐” ⑤二氧化硫可作为漂白剂 A.①②③ B.①②③④ C.①②③⑤ D.全部 二、选择题(每题只有一个选项符合题意,每题4分,共15题,计60分) 11.下列说法正确的是(设NA为阿伏加德罗常数) A.在0.1mol/L的Fe2(SO4)3溶液中,含有的Fe3+的数目为0.2NA B.将含0.2NA个NO分子的气体和含0.2NA个O2分子的气体相混合,在标准状况下的体积为8.96L C.7.1gCI2参加反应作氧化剂时,得到的电子数为0.1NA D.Imol Na跟0.4mol O2充分反应,转移的电子数为NA
A.硅酸钠(Na2SiO3) B.碳酸钠(Na2CO3) C.硫酸钠(Na2SO4) D.三聚磷酸钠(Na5P3O10) 13.大麦的一个染色体组有7个染色体,在四倍体大麦根尖细胞有丝分裂后期,能观察到的染色体数目是 A.7个 B.14个 C.28个 D.56个 14.将植物培养在(NH4)2SO4溶液中,时间一长,溶液pH值将 A.比原来的大 B.不发生任何变化 C.比原来的小 D.无法判断 15.在玉米胚和胚乳发育中,当胚囊中形成多数游离胚乳核时,受精卵则 A.发育成球状胚体 B.发育成胚 C.发育成顶细胞和基细胞 D.处在休眠状态 16.某溶液中含有HCO3-、SO32 -、AIO2-、OHˉ等4种离子。若向其中加入Na2O2后,溶液中的离子浓度基本保持不变的是 A.HCO3- B.SO3 2 - C.AIO 2- D.OH - 1 7.下列说法中正确的是 A.物体的机械能越大,则其内能也越大
B.N个分子的内能为E,则每个分子的内能为
C.物体的内能变化了,而其温度不一定变化 D.相同质量和温度的氢气和氧气内能是相等的 18.如图所示,为波沿着 一条右端固定的绳子 传播到B点的波形 示意图,由图可能判断出A开始振动的方向是 A.向左 B.向右 C.向上 D.向下
20.在恒容密闭容器中进行如下反应:N2+3H2 2NH3+Q(Q>0),温度一定时,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是 A.平衡不发生移动 B.平衡向正反应方向移动 C.NH3的百分含量减少 D.正反应速率增大,逆反应速率减少 21.下列叙述正确的是 ①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率, ②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀 ③电镀时,应把镀件置于电解槽的阴极 ④冶炼铝时,把氧化铝加入液态冰晶石中成为熔融体后电解 ⑤钢铁表面常易锈蚀生成Fe2O3﹒nH2O A.①②③④⑤ B.①③④⑤ C.①③⑤ D.②④ 22.赤道上某处有一竖直的避雷针,当带有正电的乌云经过避雷针的上方时,避雷针开始放电,则地磁场对避雷针的作用力的方向为 A.正南 B.正东 C.正西 D.正北 23.如图所示,光滑斜面的顶端有 一小球,若给小球一水平初速 度,经过时间t1小球恰落在斜 面底端;若将小球放在斜面 顶端由静止释放,小球滑至斜面底端所用时间为t2,则t1、t2的大小关系为
A.t1<t2 B.t1 >t2 C.t1=t2 D.t1=2t2
将开关S扳向a,给电 容器充足电后,再把 开关扳向b,经过时 间t电容器放电完 毕,在这一过程中放电电流的平均值为I。如果把电池组的电动势增大到原来的2倍,重复上述过程时,放电过程所用时间和放电电流的平均值应分别为 A.2t,2I B.t,21 C.2t,I D.t,I
A.新核和粒子做圆周运动的轨迹圆相内切 B.若粒子逆时针运动,新核将顺时针运动 C.新核与粒子分离后,轨道半径大的先回到M点 D.新核的动能大于粒子的动能 三、选择题(每题有1-2个选项符合题意,每题4分,共10题,计40分。若正确答案有2个选项,只选一个且正确的得2分,选2个且正确的得4分;只要出现错误选项,该小题就为0分)。 26.从塔顶以4m/s的初速度竖直上抛一个质量为2kg的小球,不计空气阻力,经过一段时间,小球的速度大小变成6m/s,对这段时间有关物理量的描述,下述正确的是 A.重力做功为20J B.重力的冲量为20N﹒s C.重力的平均功率为120W D.球的动量变化了4kgm/s
的初速度v0沿中线进 入水平放置的平行金 属板内,恰好沿下板的 边缘飞出,已知板长为 L,板间电压为U,带电粒子的带电量为q,粒子通过平行金属板的时间为T,不计粒子的重力,则
A.粒子在前 时间内,电场力对粒子做功为 qU
C.粒子在下落前 和后 内,电场力做功之比为1︰1
D.粒子在下落前 和后 内,通过的时间之比为1︰3
A.
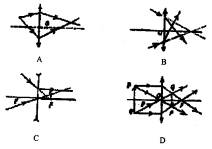
29.1g氢气完全燃烧生成液态水,放出142.9KJ的能量,下列表示该反应的热化学方程正确的是 A.H2(气)+1/202(气)═H2O(液)+285.8KJ B.2H2(气)+O2(气)2═2H2O(液)+142.9KJ C.2H2+O2═2H2O+571.6KJ D.2H2(气)+O2(气)═2H2O(气)-571.6KJ 30.假定两个生物体的基因型分别为AaBb和aaBb(位于两对同源染色体上),它们杂交产生的子代中,可能出现的表现型及基因型有 A.各有4种 B.4种和6种 C.各有6种 D.6种和8种 31.下面关于人体代谢过程的叙述中,正确的是 A.一切营养物质都要经过消化才能吸收 B.营养物质必须经过内环境才能被身体各细胞获得 C.营养物质都直接吸收到血液循环系统 D.三大有机物的代谢终产物都有水和二氧化碳 32.两只由两种材料和相同规格导线绕制的单匝矩形线圈,在同一匀强磁场中绕垂直于磁场方向的转轴匀速转动,产生的感应电动势分别是e1=10sin100πt(V)、e2=10sin200лt(V), 以下说法正确的是 A.它们经过空间同一位置时的磁通量一定相等 B.它们在同一时刻的感应电动势一定相等 C.它们在同一时刻的感应电流一定相等 D.它们的电动势的有效值一定相等 33.根据已有的化学知识和右图 所示的装置,可制备的气体是 A.用H2O2的水溶液跟MnO2 反应制取O2 B.用浓硝酸跟亚硫酸钠粉末 反应制取SO2 C.用电石跟饱和食盐水反应 制取C2H2 D.用稀硫酸跟石灰石反应制 取CO2 34.在物质的量浓度均为0.01摩/升的CH3COOH和CH3COONa混合溶液中,测得[CH3COO-]>[Na+],则下列的关系式不正确的是 A.[H+]>[OH-] B.[H+]<[OH-] C.[CH3COO-]>[CH3COOH] D.[CH3COOH]+[CH3COO-]=0.02摩/升 35.如图所示的各透镜光路图正确的是
第Ⅱ卷(非选择题,共130分) 四(本题包括7小题,共54分)
36.(7分)下表为某人早晨空腹时的尿液、原尿、血浆化验单,依表回答:
(3)当前运用现代基因工程技术,在大肠杆菌上合成了人类胰岛素。试问:决定胰岛素的氨基
(5)不同种生物之间基因移植成功,说明生物共有一套相同 。
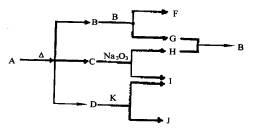
37.(6分)A~J是中学化学教材中常见的物质,A~J有如下转化关系,J是不溶于水的白色固体,且式量为100。
(2)B和E反应的化学方程式是 。
,P质点在X1轴 上做简谐振动,Q1
它们从同一高度自由下落,途中经过一个有边界的匀强磁场区域,磁场方向垂直面向里,如 图所示,若下落过程中线框平面始终与磁场方向保持垂直,不计空气阴力,则M、N底边进
框M、N内产生的热量QN= 。
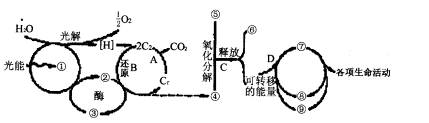
40.(7分)下图为植物体内与能量有关的生理活动图解,据图回答:
(2)1摩尔物质④完全氧化分解约有 %的能量转移到⑦中。
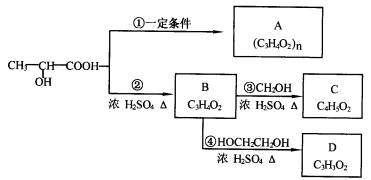
(5)请简要说明判断一成熟植物细胞死活的理论依据。 41.(10分)(1)天然橡胶主要成
天然橡胶所作某种相应的处理 后的结果,这种处理的措施是 。
用化学方法对乳酸进行加工处理的过程: 请填写以下空白: ②的反应类型是 ;化合物A的结构简式是 。
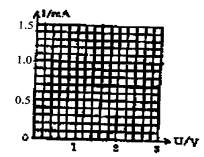
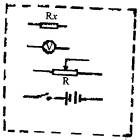
(甲) 的内阻约为20kΩ,电流表的内阻约为20Ω,变阻器的全电阻为30Ω,选择尽量减少误差的电路线接进行实验,测得各种数据用实心圆点标于坐标图上, 如甲图所示。
(乙) 五、(本题包括2小题 ,每题12分,共24分) 43.(12分)有一质量为M的气缸平放在光滑的水平面上静止不动,质量为m的活塞把一定 质量的理想气体封闭在气缸中,气柱长为L,活塞被销子固定,如图所示,已知大气压为P0,封闭气体的压强为2P0,拔掉销子,活塞能达到的最大速度为v1,若这一过程中气体的温度不变,活塞与气缸之间摩擦不计,求活塞达到最大速度时: ①气缸的速度V2;②气柱的长I4 ; ③气缸移动的距离S及这一过程中气体吸收的热量Q。 44.(12分)某学校课外活动小组从海带中提取海碘,拟定如下实验步骤并进行实验: ①将海带剪碎放在坩埚中,并用少量酒精润湿海带,用酒精灯灼烧盛有海带的坩埚,至海带完全成灰。 ②将海带灰转移到小烧杯中,加水煮沸,使可溶物溶解并过滤。 ③用淀粉溶液检验滤液是否含碘单质,观察现象。 ④向滤液中滴入几滴稀硫酸酸化滤液,再加入任选试剂A(A试剂是锌粉、亚硫酸氢钠溶 液、浓三氯化铁溶液、3%过氧化氢溶液、高锰酸钾溶液、碘化钾溶液中的一种),观察现象。 ⑤再用淀粉溶液检验滤液,观察现象。 ⑥向滤液中加入四氯化碳,振荡,静置,分液,得到碘的四氯化碳溶液。 回答下列问题: (1)步骤①中将海带剪碎并用少量酒精润湿海带,其目的是 ;
(4)在一定温度下,溶液溶解在两种接触但互不溶解的溶剂中的浓度之比是一个常数K。若CA、CB(g• L-1)分别表示溶质在A、B两种溶剂中的浓度,则有CA/CB=K,对于溶质碘而言:[CCl4/CH20=85。现在2.0L碘水,其中含碘0.020g,若用CCl4为萃取剂,按两种方法萃取:第一种方法是用50mLCCl4萃取一次;第二次方法是分两次萃取,每次用25 mLCCl4。求两种情况下水中残余的碘的质量,并指出哪种方法好。 六、(本题包括3小题,计52分) 45.(16分)一种物质的“放射性”强弱可用放射性活度来加以表示,任何量的放射性元素在1s内发射3.70×1010个α粒子或β粒子(相当于1geq o(sup 5(226),sdo 2( 88))226 88Ra在1s内放出的α粒子的数目),其放射性活度为1居里(Ci)。利用放射性同位素进行标记原子的应用范围非常广泛。例如,化学反应的微观过程的研究、医学检验、辐射育种等等。 试回答以下问题:
(3)(3分)如何证明溶解于苯的HCl分子与苯分子中的H原子之间不断地发生着氢交换。 (4)(2分)在植物的光合作用中,若用H218O和CO2为原料,此过程中所生成的O2相对分子质量为 。
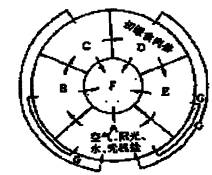
46.(26分)阅读下面材料,并回答问题。 铝可以从铝土矿中获取。铝土矿是不纯净的铝的氧化物(杂质为Fe2O3和SiO2),它是非再生资源。假如我们对铝的消费保持现有的速度,我们能获得生产足够的铝所需的铝土矿仅能维持30年左右。由此看来,保护现在自然资源和对非再生资源的再利用,是值得我们考虑的。但在废物回收过程中,仍有相当大的难度,其关键的因素主要涉及旧金属的收集、与其它废物的分离、回收和提炼金属的费用、金属本身的价值等。(已知1mol电子电量约为105C) (1)(4分)试说明回收铝的过程中存的困难。 (2)(4分)为什么金的回收率比铝的回收率要大的多? (3)(6分)常温下,SiO2与强碱或强酸是很难反应的。现利用盐酸、氢氧化钠溶液、氮气、二氧化碳和水,从铝土矿中提取纯净的Al2O3。试设计一个适用于工业生产上提纯Al2O3的实验方案。用化学方程式表示提纯的过程: (4)(3分)制取1molAl需要多少库仑的电量? (5)(3分)假定用6V的直流电源供电,进行电解,制2.7tAl需要多少千焦的电能?(请列式并计长算) (6)(3分)在1.01×105Pa,27℃时,每产生1摩Al,理论上在阳极生成氧气的体积为多少升?(请列式并计算)(小数点后保留一位数字,下同) (7)(3分)如果每度电的费用为0.60元,试计算生产厂家每生产1t Al需付出的电费为多少元(1度电=3600千焦)?(请列式并计算) 47.(10分,每空1分)下图是一个生态系统内各成分的互相联系图。请据图回答: (1)【B】、【C】、【D】、【E】为【F】提供 ,
(5)若【A】中有农药六六六(C6H6CI6)请写出它的结构简式: 。
|
教育最重要的是使人变得更聪明。教育就是要开启人的心智,使人身体好,更主动、积极,行动能力强,更能干。
中文域名: 古今中外.com
英文域名: www.1-123.com
丰富实用的教育教学资料

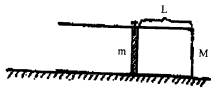
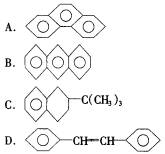 19.下列分子中,14个碳原子不可能处于同一平面的是
19.下列分子中,14个碳原子不可能处于同一平面的是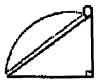
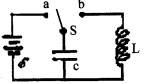 24.如图所示的电路中,
24.如图所示的电路中, 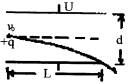 27.带正电的粒子以一定
27.带正电的粒子以一定 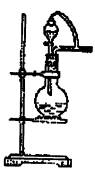
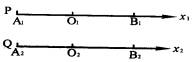 38.(6分)如图所示
38.(6分)如图所示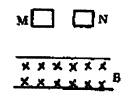
 分是 , 其
分是 , 其