高一上学期期末考试化学试卷
满分:100分 时间:1小时40分
说明:
1.本试卷分第I、II两部分,第I部分为选择题,第II部分为非选择题。
2.本试卷可能用到的相对原子质量:Mn—55 Ag—108 Cl—35.5 C—12 O—16 H—1
第Ⅰ卷(选择题,共40分)
一、选择题(本题包括20小题,每小题2分,共40分。每小题只有一个选项符合题意)
1.目前,全球有16亿人有不同程度的缺碘现象,其中包括6亿儿童。科研表明,人的一生只要能摄入一小茶匙的碘就能正常发育,健康生活。目前预防缺碘的有效办法是食用含碘食盐。这种食盐含
A.单质碘(I2) B.碘化钠中化合态的碘(I-)
C.碘酸钠中的碘元素 D.氯化碘(ICl)中的碘元素
2.下列说法正确是的
A.常温常压下,22.4L氖气含有NA个氖原子
B.1molNa2O2固体跟足量CO2的气体完全反应转移NA个电子
C.将CO2通入漂白粉溶液中一定有沉淀生成
D.焰色反应属于化学变化
3.为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的是 A.加热,观察是否有气体放出 B.溶于水后加石灰水,看有无沉淀
C.溶于水后加BaCl2溶液,看有无沉淀 D.加热后称量,看质量是否变化
4.将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为
A.5a/b mol/L B.10a/b mol/L C.b/5a mol/L D.a/b mol/L
5.在通常情况下,下列气体不能共存的是
A.H2、Cl2 B.H2、O2 C. H2、Br2 D.H2、F2
6.把CO2通入下列饱和溶液中,最终会有沉淀的是
A.CaCl2 B.Na2CO3 C.Ca(OH)2 D.NaNO3
7.下列各组物质互相作用时,生成物不随反应条件或反应物的量变化而变化的是
A.Na和O2 B.NaOH和CO2
C.NaHCO3和NaOH D.Na2CO3和HCl
8.可用离子方程式H OH-==H2O表示的化学反应是
A.CH3COOH NaOH==CH3COONa H2O
B.2HNO3 Mg(OH)2==Mg(NO3)2 2H2O
C.H2SO4 Ba(OH)2==BaSO4↓ 2H2O
D.2HCl Ba(OH)2==BaCl2 2H2O
9.下列微粒不具有还原性的是
A.H2 B.H C.Na D.CO
10.下列反应不属于氧化还原反应的是
A.Zn+2HCl=ZnCl2+H2↑
B.Ca(ClO)2+2HCl=CaCl2+2HClO
C.Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O
D.3Cl2+6KOH(浓) ![]() 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O
11.现有下列试剂:(1)氯水 (2)Br2水 (3)碘水 (4)碘酒 溶液,其中能使淀粉碘化钾溶液变蓝的是
A.除(3)外 B. 除(4)外 C. 除(2)外 D.全部
12.关于新制的氯水和久置的氯水,说法不正确的是
A.新制的氯水呈黄绿色,久置的氯水无色
B.新制的氯水漂白作用强,久置的氯水漂白作用很弱或消失
C.新制的氯水中没有氯离子,久置的氯水中才含有氯离子
D.新制的氯水中含氯气多,久置的氯水中含有极少量的氯气或不含氯气
13.既能导电又是电解质的是
A.蔗糖溶液 B.氢氧化钾溶液
C.熔融的氯化钠 D.硫酸溶液
14.根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是
①Cl2 2KI=I2 2KCl ②2FeCl3 2HI=I2 2FeCl2 2HCl
③2FeCl2 Cl2=2FeCl3 ④I2 SO2 2H2O=2HI H2SO4
A.Cl2>I2>Fe3 >SO2 B.Fe3 >Cl2>I2>SO2
C.Cl2>Fe3 >I2>SO2 D.Cl2>Fe3 >SO2>I2
15.下列物质中,不能与CO2反应的是
A.K2O2 B.RbHCO3 C.Na2O D.LiOH
16.在无土栽培中,配制内含0.5 molNH4CI,0.16 mol KCl, 0.24mol K2SO4的某营养液,若用KCl,NH4CI和(NH4)2SO4三种固体配制,则需此三种固体的物质的量分别为
A.0.40mol 0.50mol 0.12mol B.0.66mol 0.50mol 0.24mol
C.0.64mol 0.50mol 0.24mol D.0.64mol 0.02 mol 0.24mol
17.某同学在实验室用17.4g MnO2和50mL 8mol/L浓盐酸加热制Cl2,在常温常压下,该同学可制得Cl2
A.2.24L B.0.2mol C.7.1g D.无法计算
18.在标准状况下,将V L A气体(摩尔质量为Mg/mol)溶于0.1 L水中,所得溶液密度为d g·mL-1,则此溶液的摩尔浓度为
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
19.下列说法正确的是
A.标准状况下22.4L/mol就是气体摩尔体积
B.非标准状况下,1mol任何气体的体积不可能为22.4L
C.标准状况下22.4L任何物质都约含有6.02×1023个分子
D.1mol H2和O2的混合气体在标准状况下的体积约为22.4L
20.某温度下,将C12通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为
A.21:5 B. 11:3 C.3:1 D.4:1
第Ⅱ卷(非选择题,共60分)
二、非选择题(本题共7小题,共60分)
21.(4分)在标准状况下,4g H2,11.2L O2,1mol H2O中,所含分子数最多的是______,含原子数最多的是________,质量最大的是________,体积最小的是________。
22.(7分)标出下列反应的电子转移方向和数目,并填写有关内容:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
① 元素得电子, 元素被氧化。
②氧化剂与还原剂的物质的量比是 。
③若有7.3 gHCl被氧化,产生Cl2的质量为_______。
④离子方程式为: 。
23.(14分)A.B.C三种固体物质的焰色反应为黄色,分别跟水发生化学反应均得物质D的溶液;A跟水反应还有O2生成,B跟水反应还有H2生成,C跟水反应是化合反应:
(1)A为______________ B为______________ C为______________ D为______________
(2)由B生成A的化学方程式__________________________________________。
(3)由A变为D的化学方程式__________________________________________。
(4)由B变为D的化学方程式__________________________________________。
24.(12分)下列物质中都含有杂质(括号内为杂质),试选用合适的试剂和分离方法除去杂质。
填写下表:
含杂质的物质
除杂试剂
分离方法
反应的化学方程式
(1)Cl2(HCl)
(2)NaCl固体(NaI)
(3)NaNO3溶液(NaCl)
25.(6分)实验室配制500 mL 0.5 mol·L-1的NaCl溶液,有如下操作步骤:①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解;②把①所得溶液小心转入500mL容量瓶中;③继续向容量瓶中加蒸馏水至液面距离刻度2~3厘米处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部,与刻度线相切;④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀。
请填写下列空白:
A.实验操作步骤的正确顺序为(填序号) 。
B.本实验用到的基本仪器有: 。
C.若出现如下情况,对所配溶液浓度将有何影响?没有进行操作④ (偏高,偏低或不变);加蒸馏水时不慎超过了刻度 (偏高,偏低或不变)。
D.若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度 ;向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面 。
26.(10分)在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图: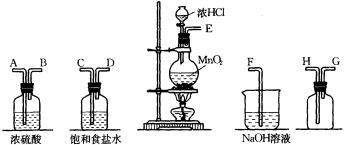
(1)连接上述仪器的正确顺序是(填各接口处的字母):E接 ,_____接 ,_____接H,G接F。
(2)在装置中:①饱和食盐水起的作用是 ,
②浓硫酸起的作用是 。
(3)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸。如果有Cl2产生,可观察到的现象是 ,写出反应方程式 。
(4)写出下列化学反应的离子方程式:
①气体发生装置中进行的反应: ;
②尾气吸收装置中进行的反应: 。
27.(7分)8.70g MnO2与100mL 37.0%密度为1.19g/cm3的浓盐酸共热(假设HCI没有损失),反应结束后,将剩余的溶液加水稀释至1000mL。取出10mL溶液加入足量AgNO3溶液,有白色沉淀生成。求
(1)反应中生成的Cl2在标准状况下的体积.
(2)10.0mL溶液加入AgNO3溶液后生成沉淀的物质的量.
高一上学期期末考试
化学试卷
参考答案
一、选择题(本题包括20小题,每小题2分,共40分。每小题只有一个选项符合题意)
1.C 2.B 3.C 4.B 5.D 6.B 7.C 8.D 9.B 10.B
11.D 12.C 13.C 14.C 15.B 16.D 17.D 18.B 19.D
20.D
二、非选择题(共60分)
21.(4分)H2 H2 H2O H2O(各1分)
22.(7分)①锰,氯;②1:5;③7.1 g。(电子转移等各1分)
④2MnO4-+16H +10Cl-=2Mn2 +5Cl2↑+8H2O(2分)
23.(14分)(1)Na2O2 Na Na2O NaOH
(2)2Na O2 Na2O2
(3)2Na2O2 2H2O==4NaOH O2↑
(4)2Na 2H2O==2NaOH H2↑(各2分)
24.(12分)
(1)饱和食盐水 洗气 略
(2)氯水 蒸发结晶
(3)AgNO3溶液 过滤
25.(6分)
A:①②④③⑤ (1分)
B:天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管(1分)
C:偏低;偏低(各1分)
D.宣告实验失败,从头重做;宣告实验失败,从头重做。(各1分)
26.(10分)
(1)CDAB(1分)
(2)除去挥发出的HCl气体,抑制Cl2在水中的溶解(1分);
吸收水蒸气,干燥Cl2(1分)
(3)试纸变蓝(1分) 2KI+Cl2=2KCl+I2(2分)
(4)MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
Cl2+2OH-=ClO-+Cl-+H2O(各2分)
27.(7分)
(1)2.24L(3分)
(2)0.008 mol(4分)
