高一化学《碱金属》单元测验试题
班级: 姓名: 学号: 得分:
可能需要的原子量 H : 1 C : 12 O : 16 Na : 23 Ca : 40
一、选择题(每题只有1个正确选项,每题4分,共48分)
1、下列反应能够生成H2的是
A、用酒精灯加热二氧化锰 B、氯酸钾的热分解反应
C、过氧化钠跟水的反应 D、把钠投入水中
2、下列属于钠离子性质的是
A、极易被氧化
B、有银白色金属光泽
C、能置换CaCl2溶液中的Ca
D、焰色反应为黄色
3、金属钠比金属钾
A、金属性弱
B、还原性强
C、原子半径大
D、原子最外层电子数少
4、碱金属熔、沸点按照元素核电荷数由小到大的顺序的递变规律是
A、由高到低 B、由低到高
C、先由低到高,再由高到低 D、先由高到低,再由低到高
5、工业上,金属钠的制备方法是
A、电解氯化钠溶液 B、电解熔融的氯化钠
C、从自然界直接开采金属钠 D、煅烧氯化钠固体
6、将2.3克金属钠投入100克水中,反应结束后,溶液中溶质的质量分数是
A、3.9% B、4.0% C、2.3% D、8.0%
7、将2.3克钠投入水中,要保证每100个水分子中溶有1个钠离子,加入的水的质量是
A、180克 B、200.8克 C、230克 D、181.8克
8、将金属钠分别投入下列物质的水溶液中,生成白色沉淀的是
A、HCl B、K2SO4 C、CuCl2 D、Ca(HCO3)2
9、对于Na2O2与H2O的反应,下列有关叙述正确的是
A、 EQ Na2O2是氧化剂,H2O是还原剂 B、Na2O2既被氧化,又被还原
C、反应过程中转移电子数为4e- D、 EQ 该反应不是氧化还原反应
10、下列离子方程式错误的是
A、小苏打溶液与烧碱溶液反应 HCO3- OH- = CO32- H2O
B、纯碱与盐酸反应 CO32- 2H = H2O CO2↑
C、小苏打溶液与盐酸反应 HCO3- H = H2O CO2↑
D、过量的二氧化碳气体通入饱和的碳酸钠溶液中 CO32- H2O CO2 = 2HCO3-
11、Na2O2与足量的NaHCO3混合后,在密闭容器中充分加热,排除气体且冷却后,残留的固体物质是
A、Na2O2和Na2CO3 B、Na2CO3
C、Na2CO3和NaOH D、Na2O2 , Na2CO3和NaOH
12、焰色反应每次实验都要用试剂洗净铂丝,这种试剂是
A、稀盐酸 B、Na2CO3溶液 C、硫酸 D、KOH溶液
二、选择题(每题只有一个正确选项,每题2分,共10分)
13、下列各组离子中,在碱性溶液中能大量共存,并且溶液为无色透明的是
A、K , MnO4- , Cl- , SO42- B、Na , HCO3- , NO3- , SO42-
C、Na , SO42- , S2- , Cl- D、K , SO42- , CO32- , SO32-
14、在一定温度下,向足量的饱和Na2CO3溶液中加入1.06克无水Na2CO3,搅拌后静置,最终所得晶体的质量是
A、等于1.06克 B、大于1.06克而小于2.86克
C、等于2.86克 D、大于2.86克
15、氢化钠(NaH)是一种白色晶体,其中钠为 1价,氢化钠和水反应放出氢气,下列叙述正确的是
A、NaH溶于水显酸性 B、NaH和水反应时,水为还原剂
C、NaH中氢离子被氧化成H2 D、NaH中氢离子最外层有2个电子
16、金属钠与金属钠在空气中的燃烧产物P分别加入到足量的水中,生成的气体在一定条件下恰好完全反应,则与水反应的金属钠与被氧化成P的金属钠的质量比为
A、1:1 B、2:1 C、23:78 D、46:78
17、有Na2CO3、NaHCO3、CaO和NaOH组成的混合物27.2克,把它们溶于足量的水中,充分反应后,溶液中的Ca2 、CO32-和HCO3-均转化为沉淀,将反应容器中的水分蒸干,最后得到白色固体共29克
A、10.6克 B、5.3克 C、5.9克 D、无法确定
请 将 选 择 题 答 案 填 入 第 3 页 的 表 格 中
(填写在其它地方为无效答案)
一、(每题4分,共48分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
二、(每题2分,共10分)
题号
13
14
15
16
17
答案
三、填空题(除标注分值外,每空1分,共22分)
18、按照核电荷数增加的顺序,碱金属元素的名称为 、 、 、 、 ,它们的符号依次是 、 、 、 、 。随着核电荷数的增加,碱金属元素原子的 逐渐增多, 逐渐增大,碱金属元素的 逐渐增强(不考虑其中的放射性元素)。 碱金属前两种元素的原子结构示意图是
、 。
19、钠容易跟空气中的 或 起反应,所以通常保存在 里;氧化钠是 色固体,过氧化钠是 色固体;在呼吸面具里有时用到过氧化钠,请写出有关的主要方程式: (2分)。
四、分析推断题(除标注分值外,每空1分,共10分)
20、 一小块金属钠投入水中,观察到:
= 1 \* GB2 ⑴ 钠浮在水面上,说明: ;
= 2 \* GB2 ⑵ 钠熔成光亮的小球,在水面上四处游动,说明:
;
= 3 \* GB2 ⑶ 反应后的水溶液中加入酚酞试剂呈红色,说明: 。
21、工业上可以CO2、NH3、H2O和NaCl为原料来生产两种固体化工产品。已知:CO2 NH3 H2O = NH4HCO3,且在一定温度下,NH4Cl、NaCl、NH4HCO3和NaHCO3的溶解度存在着这样一种关系: NaCl > NH4Cl > NH4HCO3 > NaHCO3.据此可分析得知,该两种固体化工产品分别为 和 ,其中,前者是通过 加热得到的,后者可作化学肥料。
22、向含a克NaOH的溶液中,缓慢通入b克CO2气体,充分反应后,在低温低压下蒸发溶液,得到不含结晶水的白色固体。白色固体有四种可能组成,请填写下表(在a/b的取值范围和其对应的白色固体组成均正确时,才计分。每组1分,共4分)。
a/b的取值范围
白色固体组成
1
2
3
4
四、计算题(共10分)
23、将20克Na2CO3和NaHCO3的混合物加热到质量不再减少时为止,称得剩余固体的质量为13.8克,求原混合物中NaHCO3的质量分数。(正确使用差量法,计满分7分;正确使用其它方法,计4分)
24、取5.4克由某碱金属R及其氧化物R2O组成的混合物。该混合物与足量的水反应。反应完毕,蒸发反应后得到的溶液,得到8克无水晶体。试通过计算,判断该金属是哪一种碱金属?(同时写出正确的结果和完整的判断过程,计满分3分;否则不计分)
高一化学《碱金属》单元测验试题参考答案
一、选择题(每题只有1个正确选项,每题4分,共48分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
D
D
A
A
B
A
D
D
B
D
B
A
二、选择题(每题只有一个正确选项,每题2分,共10分)
题号
13
14
15
16
17
答案
CD
D
CD
A
A
三、填空题(除标注分值外,每空1分,共22分)
18、按照核电荷数增加的顺序,碱金属元素的名称为 锂 、 钠 、 钾 、 铷 、 铯 ,它们的符![]()
![]()
![]()
![]()
![]() 号依次是 Li 、 Na 、 K 、 Rb 、 Cs 。随着核电荷数的增加,碱金属元素
号依次是 Li 、 Na 、 K 、 Rb 、 Cs 。随着核电荷数的增加,碱金属元素![]()
![]()
![]() 原子的 电子层数 逐渐增多, 原子半径 逐渐增大,碱金属元素的 金属性 逐渐增强(不考虑其中的放射性元素)。碱金属前两种元素的原子结构示意图是(略)
原子的 电子层数 逐渐增多, 原子半径 逐渐增大,碱金属元素的 金属性 逐渐增强(不考虑其中的放射性元素)。碱金属前两种元素的原子结构示意图是(略)
![]()
![]()
![]() 19、钠容易跟空气中的 氧气 或 水蒸气 起反应,所以通常保存在 煤油 里;氧化钠是
19、钠容易跟空气中的 氧气 或 水蒸气 起反应,所以通常保存在 煤油 里;氧化钠是![]()
![]() 白色固体,过氧化钠是 淡黄色固体;在呼吸面具里有时用到过氧化钠,请写出有关的主要方程式: 2Na2O2 2CO2 = 2Na2CO3 O2 (2分)。
白色固体,过氧化钠是 淡黄色固体;在呼吸面具里有时用到过氧化钠,请写出有关的主要方程式: 2Na2O2 2CO2 = 2Na2CO3 O2 (2分)。
四、分析推断题(除标注分值外,每空1分,共10分)
20、 一小块金属钠投入水中,观察到:
![]() = 1 \* GB2 ⑴ 钠浮在水面上,说明: 钠的密度比水小 ;
= 1 \* GB2 ⑴ 钠浮在水面上,说明: 钠的密度比水小 ;
![]() = 2 \* GB2 ⑵ 钠熔成光亮的小球,在水面上四处游动,说明: 钠与水反应放热,且钠的熔点较
= 2 \* GB2 ⑵ 钠熔成光亮的小球,在水面上四处游动,说明: 钠与水反应放热,且钠的熔点较![]() 低,反应中有气体生成 ;
低,反应中有气体生成 ;
![]() = 3 \* GB2 ⑶ 反应后的水溶液中加入酚酞试剂呈红色,说明: 有可溶性碱生成 。
= 3 \* GB2 ⑶ 反应后的水溶液中加入酚酞试剂呈红色,说明: 有可溶性碱生成 。
21、工业上可以CO2、NH3、H2O和NaCl为原料来生产两种固体化工产品。已知:CO2 NH3 H2O = NH4HCO3,且在一定温度下,NH4Cl、NaCl、NH4HCO3和NaHCO3的溶解度存在着这样一种关系: NaCl > NH4Cl > NH4HCO3 > NaHCO3.据此可分析得知,该![]()
![]() 两种固体化工产品分别为 Na2CO3 和 NH4Cl ,其中,前者是通过 NaHCO3 加热得到的,
两种固体化工产品分别为 Na2CO3 和 NH4Cl ,其中,前者是通过 NaHCO3 加热得到的,![]() 后者可作化学肥料。
后者可作化学肥料。
22、向含a克NaOH的溶液中,缓慢通入b克CO2气体,充分反应后,在低温低压下蒸发溶液,得到不含结晶水的白色固体。白色固体有四种可能组成,请填写下表
a/b的取值范围
白色固体组成
1
(0 , 10/11]
NaHCO3
2
(10/11 , 20/11)
NaHCO3和Na2CO3
3
20/11
Na2CO3
4
(20/11 , ∞)
NaOH和Na2CO3
四、计算题(共10分)
23、将20克Na2CO3和NaHCO3的混合物加热到质量不再减少时为止,称得剩余固体的质量为13.8克,求原混合物中NaHCO3的质量分数。(正确使用差量法,计满分7分;正确使用其它方法,计4分)
解:设原混合物中NaHCO3的质量为k,则由
|
2NaHCO3 === Na2CO3 H2O(g) CO2↑ Δm(s) |
|
Δ |
|
2×84 |
|
62 |
|
k |
|
20 – 13.8 = 6.2 |
|
得 k = 16.8(克) |
|
故 %m(NaHCO3) = (16.8/20) × 100% = 84% |
|
答:原混合物中NaHCO3的质量分数为84% |
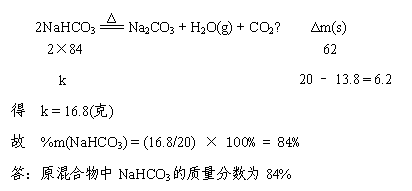 |
24、取5.4克由某碱金属R及其氧化物R2O组成的混合物。该混合物与足量的水反应。反应完毕,蒸发反应后得到的溶液,得到8克无水晶体。试通过计算,判断该金属是哪一种碱金属?(同时写出正确的结果和完整的判断过程,计满分3分;否则不计分)
解:(i) 若5.4克混合物都是碱金属R,则由
|
R ~ ROH |
|
k |
|
k 17 |
|
5.4 |
|
8 |
|
(式中,k为碱金属R的式量) |
|
得 k ≈ 35.3 |
|
R2O ~ 2ROH |
|
2k 16 |
|
2k 34 |
|
5.4 |
|
8 |
|
得 k ≈ 10.7 |
 |
(ii) 若5.4克混合物都是碱金属R的氧化物R2O,则由
综(i)和(ii)所述,碱金属R的式量k的范围为(10.7,35.3)。在碱金属中,只有金属Na的式量23在(10.7,35.3)中,所以该碱金属是金属钠。
