高一化学12月统练试卷
说明:
(1)本试卷包括第Ⅰ、Ⅱ卷,满分100分。考试时间为100分钟。
(2)可能用到的相对原子量: Li 7 C 12 N 14 O 16 F 19 Na 23 Mg 24
Al 27 S 32 K 39 Ca 40 Fe 56 Cu 64 Ag 108 Ba 137
第Ⅰ卷(共50分)
一、选择题(本题包括10小题,每小题2分。每小题只有一个选项符合题意。)
1.下列对突发事件的处理方法错误的是
A、夜间察觉液化气、煤气泄漏,应立即开灯检查
B、洒出的酒精在桌面上燃烧起来,应立即用湿抹布扑灭
C、浓硫酸不慎沾到皮肤上,必须迅速用布擦拭后用较多水冲洗
D、当你被困在火灾区,可用湿毛巾捂住口鼻,匍匐前进,寻找安全出口
2.废旧计算机的某些部件含有Zn、Fe、Cu、Ag、Pt(铂)、Au(金)等金属,经物理方法初步处理后,加入足量稀盐酸充分反应,再过滤,所得的固体中不应有的金属是 A、Cu Ag B、Zn Fe C、Pt Cu D、Ag Au
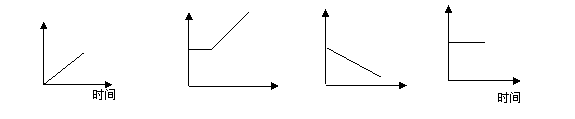
3.红磷在密闭容器(含有空气)内燃烧,容器内有关的量随时间变化的图象正确的是
|
时间 |
|
原子种类 |
|
元素种类 |
|
原子个数 |
|
时间 |
|
物质总质量 |
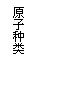     |
| |||
| |||
A B C D
![]()
![]()
![]()
![]()
![]() 4.下面是一些物质粒子的示意图,“ ”、“ ”、“ ”分别代表不同种类元素的原子,其中可能属于氧化物的是
4.下面是一些物质粒子的示意图,“ ”、“ ”、“ ”分别代表不同种类元素的原子,其中可能属于氧化物的是
![]()
![]() A、 B、 C、 D、
A、 B、 C、 D、
5. 用1kg溶剂中所含溶质的物质的量表示的溶液浓度叫质量物质的量浓度,其单位是mol/kg。某物质溶液质量分数为20%,质量物质的量浓度为2.5mol/kg,则该物质可能为
A、NaHCO3 B、KHCO3 C、CaCO3 D、Na2CO3
6. 据报道,德国INTEGRAL公司因研究出无氟冷却技术(用水和冰组成的两相液-固体代替传统的氟里昂)而荣获该年度环境大奖。关于“新制冷剂”,以下叙述错误的是
A、该制冷剂对环境不产生污染
B、该制冷剂的作用原理与氨基本相同
C、该制冷剂在水的凝固点附近的温度下发挥作用
D、该制冷剂是属于悬浊液的一种混合物
7.下列氧化还原反应中,水作氧化剂的是
A、2Na2O2+2H2O=4NaOH+O2↑ B、2F2+2H2O=4HF+O2
C、CO+H2O=CO2+H2 D、3NO2+H2O=2HNO3+NO
8.下列叙述可证明甲酸是弱电解质的有:
A、1 mol/L甲酸溶液的c(H )=0.01mol/L
B、在相同浓度时,甲酸溶液的导电性比硫酸弱
C、10mL1mol/L甲酸恰好与10mL1mol/LNaOH完全反应
D、甲酸能与水以任意比例互溶
9. 由NaHS、MgSO4、NaHSO3组成的某混合物中氧元素的质量分数为a%,该混合物中的硫元素的质量分数为
A、a% B、2 a% C、4/7(1- a%) D、1- 0.75a%
10.下列说法正确的是(NA表示阿佛加德罗常数的值)
A、SiO2晶体中, 有NA个Si就有2NA个Si—O键
B、P4分子中P原子数和P—P键数之比为3∶2
C、常温常压下,1molOH-所含电子数为10NA
D、在10.6gNa2CO3固体中CO32-数目小于0.1 NA
二、选择题(本题包括15小题,每题2分,每小题有一个或两个选项符合题意。)
12.2005年10月12日,中国“神舟六号”载人飞船顺利升空,5天后又安全着落。在升空和着落时,为了防止飞船与大气层摩擦产生高温而燃烧,应该选择某种特殊材料覆盖在飞船表面,这种材料应该具有的性质是
A、良好的导电性
B、密度较大以增大飞船的惯性
C、熔点不太高但化学性质稳定
D、质地柔软以利于飞船的变形
13.若在飞船的太空实验室中进行以下实验,其中最难完成的是
A.将金粉和铁粉混合 B.将牛奶加入水中混合
C.蒸发食盐水制取食盐晶体 D.用漏斗、滤纸过滤除去水中的泥沙
14. 下列离子方程式书写正确的是
A、氨水吸收少量的SO2 :NH3•H2O SO2 = NH4 HSO3—
B、在含n mol FeBr2溶液中通入n molCl2 :2Fe2 2Br— 2Cl2 = 2Fe3 Br2 4Cl—
C、Ca(HCO3)2溶液中加等物质的量NaOH:Ca2 2HCO3— 2OH— =CaCO3↓ CO32— 2H2O
D、在漂白粉溶液中通过量CO2气体 Ca2 2ClO— CO2 H2O = CaCO3↓ 2HClO
15.将体积都为10 mL, c(H )=0.001mol/L的盐酸和醋酸,加水稀释至amL 和bmL,测得稀释后溶液的c(H )=0.000001mol/L。则稀释后溶液的体积:
A、a=b=100 mL B、a=b=1000mL C、a<b D、a>b
16.人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变成Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有
A、酸性 B、碱性 C、氧化性 D、还原性
17.某无色气体,可能含HCl、 CO2 、NO2 、HI、 SO2 、HBr的一种或几种。
将其通入氯水中,得到无色透明溶液,把溶液分成两份,向一份中加入盐酸酸化
BaCl2溶液,出现白色沉淀,另一份加入硝酸酸化的AgNO3溶液,也有白色沉淀。
对于原无色气体推断定正确是
A、一定存在HCl B、一定存在SO2
C、可能有CO2 D、不能肯定是否含有NO2、HI
18.在反应a BrF3 b H2O = c HBrO3 d Br2 e HF f O2 中(a、 b 、c、 d、 e、 f是各物质的化学计量数),若0.3mol H2O被氧化,则被水还原的 BrF3 的物质的量是
A、0.3mol B、 0.2mol C、0.4mol D、 0.5mol
19.在某无色酸性溶液中,能大量共存的离子组是
A、NH4+、Mg2+、SO42-、Cl- B、Ba2+、K+、Cl-、NO3-
C、Al3+、Cu2+、SO42-、Cl- D、Na+、Ag+、Cl-、AlO2-
20.含amolHCl的浓盐酸与足量MnO2反应制得bmolCl2,已知稀盐酸不能被MnO2氧化成氯气,则下列关系正确的是( )
A、a=4b B、a=2b C、a<2b D、a>4b
21.将一小块金属钾投入到CuSO4稀溶液中,可观察到的现象是
①钾浮在液面上②钾熔化成银白色小球③发出嘶嘶的声音④甚至有轻微的爆炸声⑤有红色沉淀析出⑥生成蓝色沉淀
A、①②③④⑤ B、①③⑤⑥ C、①②③④⑥ D、全部
22.下列元素的含量由多到少的排序,正确的是
A、空气中:氮、氧、碳 B、地壳中:硅、氧、铝
C、人体中:碳、氢、氧 D、海水中:氯、氢、氧
23.现有两种不含结晶水的盐,它们在不同温度下的溶解度分别是:
20℃ 50℃
A的溶解度 35.7g 46.4g
B的溶解度 31.6g 108g
下列就说法中,正确的是
A、可采用蒸发的方法提纯A物质,用重结晶的方法提纯B物质,
B、若把108gB的饱和溶液从50℃降到20℃,析出的B是76.4g
C、在20℃时,A、B都可以配成溶质质量分数为25%的不饱和溶液
D、两种盐在某一温度下可能具有相同的溶解度
24.在化学反应A+2B=C,将10gA与10gB混合,使之反应,生成15gC。与此相关的下列结论中,一定正确的是
A、反应后,A、B都有剩余B、参加反应的A为5g,B为10g
C、参加反应的A、B各为5gD、反应后,A、B中有一种物质剩余5g
25.在120℃、101.3kPa下,有由1L水蒸气,2LCO,2LCO2,0.5L氧气和1L氢气组成的混合气体。将此混合气体通过盛有足量的铜粉、足量的炭粉、足量的氧化铜粉的3只灼热反应管。假设每只管都能充分反应,而且不论这3只反应管以何种顺序排列,尾气中不可能存在的气体是
A、水蒸气 B、一氧化碳 C、氢气 D、氧气
2008年江苏省华罗庚中学高一12月统练
化学答题卷
一、二、选择题(50分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
- |
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
第Ⅱ卷(共50分)
三、实验题(本题包括2小题,共14分)
26.(1)下列实验操作正确的是 。
A、用酸式滴定管量取25.12mL的KMnO4溶液
B、用10mL量筒量取8.5mL蒸馏水
C、用pH试纸测定氯水的pH值为3.3
D、将一张湿润的蓝色石蕊试纸投入盛有Cl2的集气瓶中,试纸最终将变红
E、用坩埚加热硫酸铜溶液制取胆矾晶体
(2)下面a—f是中学生实验中常见的几种仪器(填写编号,多选倒扣分):
(a)量筒 (b)容量瓶 (c)普通试管 (d)圆底烧瓶 (e)温度计 (f)天平
(1)其中要标示仪器具体使用温度的是(不考虑温度计) ;
(2)可用作反应器并能进行加热的是 。
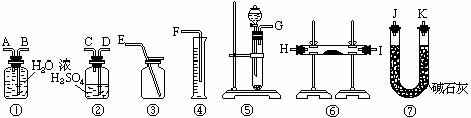
27.现有一定量含有Na2O杂质的Na2O2试样。请从下图中选用适当的实验装置,请设计一个最简单的实验,测定Na2O2试样的纯度。
(可供选择的反应物只有CaCO3固体,6mol/L盐酸和蒸馏水)。
 |
请填写下列空白:
(1)写出实验中Na2O和Na2O2分别发生反应的化学方程式。
、 ;
(2)应选用的装置是(只要求写出图中装置的标号) ;
(3)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略).
。
四、简答题(本题包括4小题,共12分)
28.含有一定量CH3COONa和CH3COOH的水溶液称作“缓冲溶液”,在该溶液中加入少量的强酸或强碱时,溶液的pH几乎不变,这可由下列离子方程式来说明:
加入酸时CH3COO- H =CH3COOH;加入碱时CH3COOH OH-= CH3COO- H2O,
由于CH3COOH和CH3COO-的大量存在,溶液中的c(H )与c(OH-)基本保持不变。
一定量的H2S和NaHS的溶液也具有缓冲作用,写出在此溶液中加入少量强酸或强碱时发生的离子反应方程式:
加入酸时 ;
加入碱时 。
29.化学反应中,如果给原子核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:原子核对核外电子的吸引力;形成稳定结构的倾向。下表是一些周期表中1-18号元素的气态原子失去核外不同电子所需的能量(kJ·mol-1):
锂
X
Y
失去第一个电子
519
502
580
失去第二个电子
7296
4570
1820
失去第三个电子
11799
6920
2750
失去第四个电子
9550
11600
① 通过上述信息和表中的数据分析:为什么锂原子失去核外第二个电子时所需的
能量要远远大于失去第一个电子所需的能量: ;
②在一定条件下,表中X可能与氢气反应的化学方程式是 ;
③Y元素常见的化合价可能是 。
30.铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它氧化性比高锰酸钾更强,本身在反应中被还原为Fe3 离子。制取铁酸钠的程式为:
Fe(NO3) NaOH Cl2─Na2FeO4 NaNO3 NaCl H2O ,则反应中 元素被氧化。
五、推断题(本题共1小题,共8分)
31.某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现图所示的物质之间的变化:
据此判断:
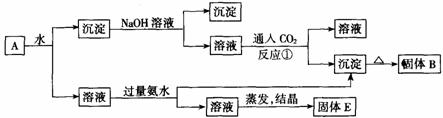
(1)固体B所含物质的化学式为______________;
(2)固体E所含物质的化学式为______________;
(3)反应①的离子方程式为____________ 。
六、计算题(本题共2小题,共16分)
32.将50mL 0.1mol/LBaCl2溶液与100mL0.75mol/L H2SO4溶液混合,求:
(1)反应产生沉淀的质量是 g;(保留2位有效数字)
(2)若不考虑溶液体积的变化,则反应后溶液的C(H+)为 。
 33.取等物质的量浓度的NaOH溶液两份A
33.取等物质的量浓度的NaOH溶液两份A
和B,每份50mL,向其中各通入一定量的CO2,
然后各取溶液10mL,分别将其稀释为100mL,
分别向稀释后的溶液中逐滴加入0.1mol/L的
盐酸,标准状况下产生CO2气体体积与所加盐
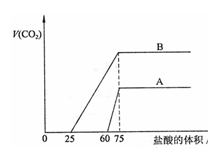
酸体积之间的关系如下图所示,试回答下列问题:
(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为) , ,两种溶质的物质的量之比为 ;加盐酸后产生CO2体积的最大值为 mL。
(2)曲线B表明,原溶液中通入CO2后,所得溶液中的溶质为 , ,两种溶质物质的量之比为 ;加盐酸后产生CO2体积最大值 mL。
(3)通过计算求NaOH溶液的物质的量浓度。
 |
答案及评分标准
一、二、选择题(50分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
A |
B |
D |
A |
B |
D |
C |
A |
C |
C |
B |
C |
D |
|
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
- |
|
B |
D |
D |
BC |
B |
AB |
D |
C |
A |
AD |
D |
D |
- |
第Ⅱ卷(共50分)
三、实验题(本题包括2小题,共14分)
26.(1)下列实验操作正确的是 A、B 。
A、用酸式滴定管量取25.12mL的KMnO4溶液
B、用10mL量筒量取8.5mL蒸馏水
C、用pH试纸测定氯水的pH值为3.3
D、将一张湿润的蓝色石蕊试纸投入盛有Cl2的集气瓶中,试纸最终将变红
E、用坩埚加热硫酸铜溶液制取胆矾晶体
(2)下面a—f是中学生实验中常见的几种仪器(填写编号,多选倒扣分):
(a)量筒 (b)容量瓶 (c)普通试管 (d)圆底烧瓶 (e)温度计 (f)天平
(1)其中要标示仪器具体使用温度的是(不考虑温度计) a、b ;
(2)可用作反应器并能进行加热的是 c、d 。
27.现有一定量含有Na2O杂质的Na2O2试样。请从下图中选用适当的实验装置,请设计一个最简单的实验,测定Na2O2试样的纯度。
(可供选择的反应物只有CaCO3固体,6mol/L盐酸和蒸馏水)。
 |
请填写下列空白:
(1)写出实验中Na2O和Na2O2分别发生反应的化学方程式。
Na2O+H2O=2NaOH 、 2Na2O2+2H2O=4NaOH+O2↑ ;
(2)应选用的装置是(只要求写出图中装置的标号) ⑤①④ ;
(3)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略).
GABF 。
四、简答题(本题包括4小题,共12分)
28.含有一定量CH3COONa和CH3COOH的水溶液称作“缓冲溶液”,在该溶液中加入少量的强酸或强碱时,溶液的pH几乎不变,这可由下列离子方程式来说明:
加入酸时CH3COO- H =CH3COOH;加入碱时CH3COOH OH-= CH3COO- H2O,
由于CH3COOH和CH3COO-的大量存在,溶液中的c(H )与c(OH-)基本保持不变。
一定量的H2S和NaHS的溶液也具有缓冲作用,写出在此溶液中加入少量强酸或强碱时发生的离子反应方程式:
加入酸时 HS- H+=H2S ;
加入碱时 H2S OH-=HS-+H2O 。
29.化学反应中,如果给原子核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:原子核对核外电子的吸引力;形成稳定结构的倾向。下表是一些周期表中1-18号元素的气态原子失去核外不同电子所需的能量(kJ·mol-1):
锂
X
Y
失去第一个电子
519
502
580
失去第二个电子
7296
4570
1820
失去第三个电子
11799
6920
2750
失去第四个电子
9550
11600
② 通过上述信息和表中的数据分析:为什么锂原子失去核外第二个电子时所需的
能量要远远大于失去第一个电子所需的能量:锂失去第一个电子后达稳定结构;
②在一定条件下,表中X可能与氢气反应的化学方程式是 2X+H2=2XH ;
③Y元素常见的化合价可能是 +3 。
30.铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它氧化性比高锰酸钾更强,本身在反应中被还原为Fe3 离子。制取铁酸钠的程式为:
Fe(NO3)3 NaOH Cl2─Na2FeO4 NaNO3 NaCl H2O ,则反应中 Fe 元素被氧化。
五、推断题(本题共1小题,共8分)
31.某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现图所示的物质之间的变化:
据此判断:

(1)固体B所含物质的化学式为__Al2O3_____;
(2)固体E所含物质的化学式为_K2SO4与(NH4)2SO4___________;
(3)反应①的离子方程式为__ Al O2-+CO2+2H2O=Al(OH)3↓+HCO3- 。
六、计算题(本题共2小题,共16分)
32.将50mL 0.1mol/LBaCl2溶液与100mL0.75mol/L H2SO4溶液混合,求:
(1)反应产生沉淀的质量是 1.2 g;(保留2位有效数字)
(2)若不考虑溶液体积的变化,则反应后溶液的C(H+)为 1. 0mol/L 。
 33.取等物质的量浓度的NaOH溶液两份A
33.取等物质的量浓度的NaOH溶液两份A
和B,每份50mL,向其中各通入一定量的CO2,
然后各取溶液10mL,分别将其稀释为100mL,
分别向稀释后的溶液中逐滴加入0.1mol/L的
盐酸,标准状况下产生CO2气体体积与所加盐
酸体积之间的关系如下图所示,试回答下列问题:
(1)曲线A表明,原溶液中通入CO2后,所得溶液中的溶质为NaOH ,Na2CO3 ,两种溶质的物质的量之比为3:1;加盐酸后产生CO2体积的最大值为 33.6 mL。
(2)曲线B表明,原溶液中通入CO2后,所得溶液中的溶质为 Na2CO3 ,NaHCO3 ,两种溶质物质的量之比为 1:1 ;加盐酸后产生CO2体积最大值 112 mL。
(3)通过计算求NaOH溶液的物质的量浓度。
解析:生成二氧化碳最多时,溶液中只有NaCl
故0.05C(NaOH)×1/5=0.075×0.1
C(NaOH)=0.75mol/L
