高一上学期化学期末试题
可能用到的相对原子质量 H 1 C 12 N 14 O 16 Na 23 Al 27
一、选择题(1—10小题每小题2分,11-20小题每小题3分,共50分)每小题只有1个
选项符合题意。
1.下列反应,不属于氧化还原反应的是 ( )
|
|
C.2Na2O2 2CO2===2Na2CO3 O2↑ D.Fe CuSO4===FeSO4 Cu
2.碘缺乏病是目前已知的导致人类智力障碍的主要原因,为解决这一全国性问题,我国已
经开始实施“智力工程”,最经济可行的措施是 ( )
A.食盐加碘 B.饮用水加碘 C.大量食用海带 D.注射含碘药剂
3.氯气可用于消毒,是因为氯气 ( )
A.具有强氧化性 B.能与水作用生成一种强氧化剂
C.有毒 D.是一种极活泼的非金属单质
4.下列物质长期露置于空气中都会变质,但不是发生氧化还原反应的是 ( )
A.Na B.NaOH C.Na2CO3 D.氯水
5.检验稀碘水和稀溴水时,所用的最佳试剂是 ( )
A.淀粉溶液 B.氯水 C.NaOH溶液 D.NaBr溶液
6.在氯水中加入KI溶液,振荡,再加入CCl4振荡后静置,观察到的现象是 ( )
A.液体呈紫红色 B.液体分两层,上层无色,下层紫红色
C.液体分两层,上层紫红色,下层无色D.液体分两层,上下均为紫红色
7.同温同压下,两种气体的体积如果不相同,其主要原因是 ( )
A.气体的分子大小不同 B.气体分子间的平均距离不同
C.气体的性质不同 D.气体的物质的量不同
8.在酸性溶液中能大量共存,并且溶液为无色透明的是 ( )
A.Na 、K 、Cu2 、SO42- B.NH4 、Na 、NO3-、Cl-
C.K 、Ca2 、HCO3-、Cl- D.Mg2 、Fe3 、Cl-、OH-
9.标准状况下有:①5.4mL H2O ②5.6L CH4 ③3.01×l023个H2S分子 ④19.6gH2SO4,这
些物质中,含分子个数由多到少的顺序是 ( )
A.③①②④ B.③①④② C.①②③④ D.④②③①
10.阿伏加德罗常数的数值等于 ( )A.12g碳所含的原子个数
B.22.4L CO所含的分子个数
C.1.01×l05 Pa、20℃时,0.5mol O2所含的原子个数
D.IL lmol/L Na2SO4溶液中 Na 的个数
11.在下列反应过程中,有3mol电子转移的是 ( )
A.lmol钠与水反应
B.27g铝与足量盐酸反应
C.22.4L氧气(标准状况)与足量镁反应
D.1.5mol Na2O2与足量水反应
12.下列叙述正确的是 ( )
A.还原性:Na>K
B.热稳定性:NaHCO3>Na2CO3
C.等物质的量的NaHCO3和Na2CO3分别跟足量盐酸反应,消耗HCl的物质的量比为1:2
D.等质量的NaHCO3和Na2CO3分别跟足量盐酸反应,产生CO2的物质的量比为1:2
13.在含有KBr和NaI的混合物中通入过量Cl2充分反应后,将溶液蒸干,并将剩余残渣
灼烧,最后留下的物质是 ( )
A.KCl B.KCl和NaBr C.KCl和KBr D.KCl和NaCl
14.某银白色金属A露置于空气中颜色逐渐变灰而生成B,B表面逐渐形成液态的C,最
后C又变成白色粉末状D。取D在无色火焰上灼烧,有黄色火焰。下列各组物质中,
按A、B、C、D顺序排列的是 ( )
A.K、K2O、K2CO3、KHCO3 B.Na、Na2O2、NaOH、Na2CO3
C.K、K2O、KOH、K2CO3 D.Na、Na2O、NaOH、Na2CO3
15.下列离子方程式书写正确的是 ( )
A.金属钠投入到水中 Na+2H2O= Na +2OH- + H2↑
B.CaCO3与盐酸反应 CO32- 2H ==CO2↑ H2O
C.Ca(OH)2与CO2反应 Ca2 2OH- CO2 == CaCO3↓ H2O
D.实验室用浓盐酸和二氧化锰反应 MnO2+2H +2Cl-==Mn2 +Cl2↑+H2O
16.已知甲烷和氧气的混合气体中,甲烷的质量分数为20%,则甲烷和氧气的体积比为
( )
A.1∶4 B.1∶5 C.1∶4.5 D.1∶2
17.R2O8n-离子在一定条件下可以把Mn2 离子氧化为 MnO4-,若反应后R2O8n-变为RO42-
离子。又知反应中氧化剂与还原剂的物质的量之比为5∶2。则n的值是 ( )
A.l B.2 C.3 D.4
18.在甲、乙、丙、丁四个烧杯中分别加人0.lmolNa、Na2O、Na2O2、NaOH,然后各加入
100mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁四个烧杯的溶液中含NaOH的
质量分数大小顺序正确的是 ( )
A.丁>丙>乙>甲 B.丙=乙>甲>丁
C.丙=乙>丁=甲 D.丙>乙>甲>丁
19.将一定量的NaHCO3和Na2CO3的混合物加热到不再放出气体时,收集到CO2 aL,冷
却后向。残余物中加入足量盐酸又收集到CO2 2aL(体积均在标准状况下测定)。则混
合物中Na2CO3和NaHCO3的物质的量之比为 ( )
A.1∶1 B.1∶2 C.1∶3 D.1∶4
20.由CO和H2组成的混合气体3.6g在足量的O2中充分燃烧后,立即通入足量的Na2O2
固体中,固体的质量增加 ( )
A.l.8g B.3.6g C.7.2g D.不可求
二、境空题(共22分)
21.(9分)新制的氯水显 色,说明氯水中有 分子存在。向氯水中滴入几滴
AgNO3溶液,立即有 生成,说明氯水中有 存在。蓝色石蕊试纸遇到
氯水后,首先变红,但很快又褪色,这是因为 。
氯水经光照后,黄绿色消失,并放出无色的 气,该反应的化学方程式是
。
22.(2分)4.6g Na放在 g水中,才能使每10个水分子中溶有一个Na 。
23.(6分)与16g氧气所含的分子数相同的氨气是 g;与16g氧气所含的原子总数相
同的氨气是 g;相同条件下,在5.6g氮气中添加 g氨气,所组成的混合气
体的体积与16g氧气所占的体积相等。
24.(5分)相同条件下,同质量的X、Y两种气体,相对分子质量分别为A、B,则它们
的体积比为 ,分子个数比为 ,密度比为 ;相同条件下的X、
Y两种气体体积相同,则X:Y的质量比为 ,物质的量比为 。
三、实验题(共16分)
25.(7分)实验室用2.0 mol/L NaCl溶液配制100mL 0.50 mol/L NaCl溶液。
(1)配制上述溶液,需要2.0 mol/L NaCl溶液 mL。
(2)配制上述溶液除需要玻璃棒、胶头滴管外,还需要的仪器有 、 、 。
(3)配制过程中出现以下情况,对所配溶液浓度有何影响(填“偏高”“偏低”“不变”)
①没有洗涤烧杯和玻璃棒。 。
②定容时俯视容量瓶的刻度线。 。
③如果加水超过了刻度线,取出水使液面恰好到刻度线。 。
26.(9分)请利用下列装置及试剂组装一套装置。其流程是,先制取纯净干燥的Cl2(不
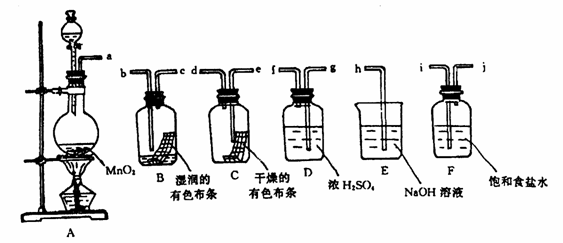 收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性。试回答:
收集),后试验干燥的Cl2和潮湿的Cl2有无漂白性。试回答:
(1)按气体从左向右流向将各装置依次连接起来(填接口标号): a 接 ,
接 , 接 , 接 , 接 。
(2)烧瓶中发生反应的化学方程式是 。
(3)D装置的作用是 ,E装置的作用是 ,
F装置的作用是 。
(4)C瓶中的现象是 ,B瓶中的现象是 。以上事
实说明起漂白作用的物质是 。
四、计算题(共12分)
27.(4分)有某温度下22%NaNO3溶液150mL,加100g水稀释后溶质质量分数变成14%。
求原溶液的物质的量浓度是多少?
28.(8分)将7.0gNa2O2和Na2O的混合物跟9.8g水充分反应后,所得NaOH溶液中含
NaOH的质量分数为50%,试计算原混合物中Na2O2和Na2O的质量。
高中学生学科素质训练
高一上学期化学参考答案
期末试题
一、
1、A 2、A 3、B 4、B 5、A 6、B 7、D 8、B 9、A 10、C 11、B
12、C 13、D 14、D 15、C 16、D 17、B 18、D 19、B 20、B
二、
|
|
H 使石蕊显红色,HClO使红色褪去。 2HClO===2HCl O2↑
22、39.6 23、8.5 5.7 5.1 24、B:A B:A A:B A:B 1:1
三、
25、(1)25.0 (2)100mL容量瓶 烧杯 量筒 (3)偏低 偏高 偏低
![]() 26、(1)i j g f e d b c h (2)MnO2 4HCl(浓)==MnCl2 2H2O Cl2↑
26、(1)i j g f e d b c h (2)MnO2 4HCl(浓)==MnCl2 2H2O Cl2↑
(3)干燥氯气 吸收多余的氯气 除去HCl气体
(4)有色布条不褪色 有色布条褪色 次氯酸(HCl)
四、
27、3.0mol/L
28、Na2O 3.1g Na2O2 3.9g
命题人:山西太原五中 崔建栋
